Eredeti cikk dátuma: 2020. április 29.
Eredeti cikk címe: Antibody responses to SARS-CoV-2 in patients with COVID-19
Eredeti cikk szerzői: Quan-Xin Long, Bai-Zhong Liu, […]Ai-Long Huan
Eredeti cikk elérhetősége: https://www.nature.com/articles/s41591-020-0897-1
Eredeti cikk státusza:
Fordító(k): Wagner Péter
Lektor(ok): dr. Serly Julianna
Nyelvi lektor(ok): Rét Anna
Szerkesztő(k): Kovács László
Figyelem! Az oldalon megjelenő cikkek esetenként politikai jellegű megnyilvánulásokat is tartalmazhatnak. Ezek nem tekinthetők a fordítócsoport politikai állásfoglalásának, kizárólag az eredeti cikk írójának véleményét tükrözik. Fordítócsoportunk szigorúan politikamentes, a cikkekben esetlegesen fellelhető politikai tartalommal kapcsolatosan semmiféle felelősséget nem vállal, diskurzust, vitát, bizonyítást vagy cáfolatot nem tesz közzé.
Az oldalon található információk nem helyettesítik a szakemberrel történő személyes konzultációt és kivizsgálást, ezért kérjük, minden esetben forduljon szakorvoshoz!
Absztrakt
Ebben a cikkben 285 COVID19-beteg SARS-CoV-2 elleni akut ellenanyagválaszáról számolunk be. A tünetek kezdete után 19 nappal a betegek 100%-ának volt pozitív a tesztje az antivirális immunglobulin-G-re (IgG). Az IgG- és IgM-szerokonverzió egyidejűleg vagy egymást követően történt. Mind az IgG-, mind az IgM-titerek a szerokonverzió utáni 6 napon belül érték el a platót. A szerológiai vizsgálatok hasznosak lehetnek a negatív RT-PCR eredményt mutató feltételezett betegek diagnosztizálásánál és a tünetmentes fertőzések azonosításánál.
Főbb tudnivalók
A 2019-es koronavírus-betegség (COVID19) folyamatos terjedése világszerte széles körű aggodalomra adott okot, és az Egészségügyi Világszervezet (WHO) 2020. március 11-én a COVID19-et világjárvánnyá nyilvánította. A súlyos akut légzőszervi szindróma (SARS) és a közel-keleti légzőszervi szindróma (MERS) vizsgálata megmutatta, hogy a vírusspecifikus ellenanyagok a betegek 80-100%-ában kimutathatók voltak a tünetek kezdete után 2 héttel (1–6). Jelen állás szerint a SARS-CoV-2-re adott ellenanyagválaszok alig ismertek, és a szerológiai vizsgálat klinikai haszna nem egyértelmű (7).
A vizsgálatba összesen 285 COVID19-beteget vontunk be három kijelölt kórházból. E betegek közül 70-nél történt egymást követően több mintavétel. A betegek jellemzőit az 1. és a 2. kiegészítő táblázatban foglaltuk össze. A vírusspecifikus ellenanyag-kimutatáshoz mágneses kemilumineszcens immunkémiai módszert (MCLIA) validáltunk és alkalmaztunk (Bővített adatok, 1a–d ábra és 3. kiegészítő táblázat). A COVID19-betegek szérummintái nem mutattak keresztreakciót a SARS-CoV tüske-antigén S1 alegységével. Ugyanakkor a COVID19-betegek szérummintái esetében keresztreakciót tapasztaltunk a SARS-CoV nukleokapszid antigénjeivel (Bővített adatok, 1e ábra). A pozitív vírusspecifikus IgG-jű betegek aránya a tünetek kezdete után 17-19 nappal elérte a 100%-ot, míg a pozitív vírusspecifikus IgM-mel rendelkező betegek aránya a tünetek kezdete után 20-22 nappal érte el a 94,1%-os csúcsot (1a ábra és Módszerek). A tünetek kezdete utáni első 3 hétben növekedést tapasztaltunk a vírusspecifikus IgG- és IgM-antitesttiterekben (1b ábra). Mindazonáltal az IgM enyhén csökkent a > 3 hetes csoportban a ≤ 3 hetes csoporttal összehasonlítva (1b ábra). A súlyos tüneteket mutatók csoportjában az IgG- és IgM-titerek magasabb szintje volt mérhető, mint a nem súlyos csoportban, bár szignifikáns különbséget csak az IgG-titerekben lehetett tapasztalni a tünetek kezdete utáni 2 hetes csoportban (1c ábra, P = 0,001).
1. ábra. A SARS-CoV-2-re adott ellenanyagválaszok.



a) A vírusspecifikus, IgG-re és IgM-re pozitív minták grafikonja a tünetek kezdete óta eltelt napok viszonylatában, 262 pácienstől származó 363 szérumminta alapján.
b) A páciensekben kimutatott SARS-CoV-2 elleni antitestek szintje a tünetek kezdetétől számított különböző időpontokban.
c) A súlyos és a nem súlyos betegekben kimutatott SARS-CoV-2 elleni antitestek szintjének összehasonlítása. A b és a c ábra box-plotjain a mediánok (középvonal) és a harmadik és negyedik kvartilis (boxok) láthatók, míg a kilengések a boxok alatti és fölötti interkvartilis tartomány (IQR) 1,5×-es értékét jelzik. Alatta látható a betegszám (N). A p-értékeket független mintás, kétoldalas Mann–Whitney U-próbával határoztuk meg.
Hatvanhárom igazolt COVID19-beteget egészen a hazabocsátásig nyomon követtünk. Háromnapos időközönként vettünk szérummintákat tőlük. Ezen mintákban az összesített szerokonverziós arányszám 96,8% (61/63) volt a követési időszakban. Két beteg, egy anya és a lánya, a kórházi kezelési időszak alatt IgG- és IgM-negatív maradt. A szerológiai folyamatokat 26 betegnél lehetett követni, akik eleinte szeronegatívak voltak, majd szerokonverzión estek át a megfigyelési időszak során. Ezekben a betegekben a tünetek kezdete utáni 20 napon belül megtörtént az IgG és az IgM szerokonverziója. A szerokonverzió mediánnapja a tünetek kezdete utáni 13. nap volt mind az IgG, mind az IgM esetében. Háromféle szerokonverziót figyeltek meg: az IgG és IgM egyidejű szerokonverzióját (kilenc beteg), az IgM korábbi szerokonverzióját az IgG-hez képest (hét beteg) és az IgM későbbi szerokonverzióját az IgG-hez képest (tíz beteg) (2a ábra). A 2b–d ábrán és a Bővített adatok 2a–c ábráján a szerokonverzió három típusát felmutató hat reprezentatív betegben lévő longitudinális ellenanyag-változások láthatók.
2. ábra. A SARS-CoV-2 elleni antitestek szerokonverziós ideje.
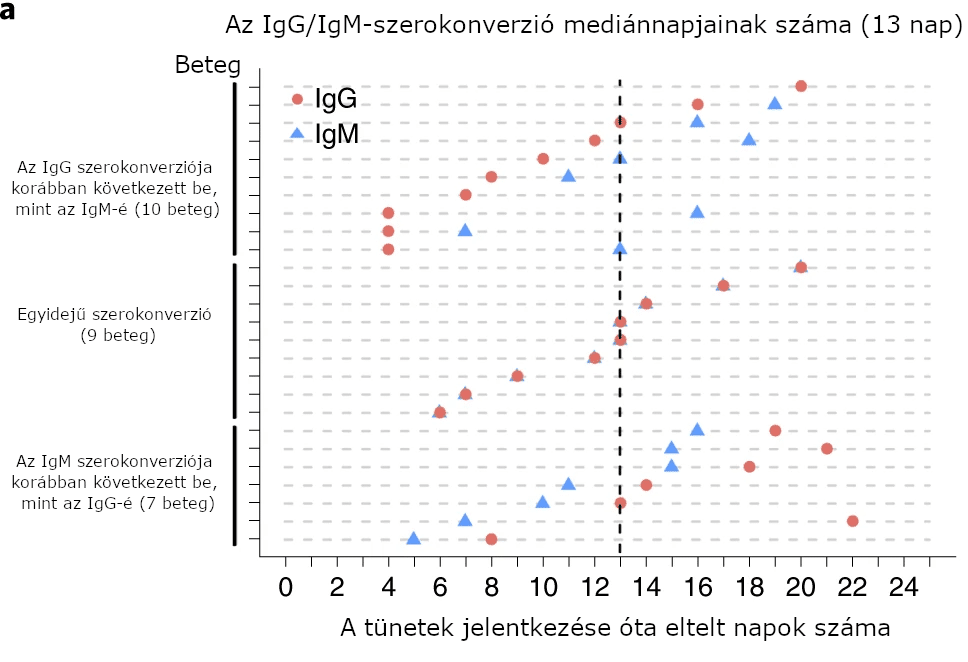



a) 26 beteg szerokonverziójának típusa, akik eleinte szeronegatívak voltak a megfigyelési időszak során. A grafikon az egyes betegek szerokonverziós napjait ábrázolja.
b–d) a három szerokonverziós típusra hat reprezentatív példa: az IgG és az IgM egyidejű szerokonverziója (b), az IgM szerokonverziója korábbi, mint az IgG-é (c) és az IgM szerokonverziója későbbi, mint az IgG-é (d).
Azon 19 beteg IgG-szintje, akiknél az IgG szerokonverziója a kórházi kezelés során megtörtént, az első pozitív IgG-mérés utáni 6. napon érte el a platót (Bővített adatok, 3. ábra). Az IgG platóértéke jelentősen (több mint 20-szorosan) eltért a betegek között. Az IgM a dinamikus változások hasonló profilját mutatta (Bővített adatok, 4. ábra). Az IgG platószintjei és a betegek klinikai jellemzői között nem találtunk összefüggést (Bővített adatok, 5a–d ábra). Ezután azt elemeztük, hogy a WHO által a MERS-CoV-fertőzés megerősítésére ajánlott kritériumok, beleértve (1) a szerokonverziót vagy (2) az IgG-specifikus antitesttiterek négyszeres növekedését, alkalmas-e a COVID19 diagnózisára (41 beteg páros mintáját alkalmazva). A kezdeti mintát a betegség első hetében gyűjtöttük be, a másodikat pedig 2-3 héttel később. Azon betegek közül, akik az IgG-re a betegség első hetében kezdetben szeronegatívak voltak, 51,2% (21/41) ment át szerokonverzión. Összesen 18 páciens volt eleinte szeropozitív a betegség első hetében; közülük nyolc páciensnél négyszeresére nőtt a vírusspecifikus IgG-titer (Bővített adatok, 6. ábra). Összességében a COVID19-betegek 70,7%-a (29/41) felelt meg az IgG-szerokonverziós kritériumoknak és/vagy az IgG-titerek négyszeres vagy ennél nagyobb növekedési kritériumának.
Annak megállapítására, hogy a szerológiai tesztelés segíthet-e a COVID19-betegek azonosításában, 52 gyanús esetet vizsgáltunk, akik a COVID19 tüneteit mutatták vagy kóros radiológiai leleteik voltak, és akiknél a virális RNS-teszt legalább két egymást követő mintában negatív volt. Az 52 gyanús esetből négynél találtunk vírusspecifikus IgG-t vagy IgM-et a kezdeti mintákban (Bővített adatok, 7. ábra). A 3. betegnél több mint négyszeresére nőtt az IgG-titer a kezdeti szerológiai vizsgálat utáni 3. napon. Érdekes módon a 3. beteg a vírusfertőzésre pozitív teszteredményt mutatott a reverz transzkripciós polimeráz láncreakcióval is (RT-PCR) két ellenanyagszint-mérés között. Az IgM-titer három egymást követő mintában növekedett az 1. betegben (< 4-szeresre). A 4. beteg két egymást követő mintájában 100-szor magasabb IgG- és tízszer magasabb IgM-titereket mértek, mint a küszöbérték. A 2. betegnek pozitív lett a vizsgálati eredménye a vírusspecifikus IgG-re és IgM-re is. Az egymást követő mintákban az IgG, illetve az IgM növekedése vagy a tünetek után 2 héttel gyűjtött egyetlen mintában a pozitív eredmény arra enged következtetni, hogy ez a három beteg SARS-CoV-2-fertőzött volt.
Továbbá bemutattuk, hogy a szerológiai tesztelés alkalmazható a felderítésre is ismert COVID19-betegek 164 közeli kontaktjának klaszterében. Tizenhat személy igazoltan SARS-CoV-2 fertőzött volt az RT-PCR alapján, és három esetben nem jelentkeztek tünetek. A többi 148 személynek negatív volt az RT-PCR eredménye, és nem jelentkeztek náluk tünetek (Bővített adatok, 8. ábra). Ettől a 164 személytől szérummintát vettünk az ellenanyagtesztekre mintegy 30 nappal a kitettség után. A 16 RT-PCR által igazolt eset mind pozitív volt a vírusspecifikus IgG és/vagy IgM esetében. Továbbá a negatív RT-PCR eredményt mutató 148 személyből 7-nek volt pozitív vírusspecifikus IgG-je vagy IgM-je, ami azt mutatja, hogy a közeli kontaktok 4,3%-át (7/164) nem sikerült azonosítani a nukleinsavteszttel. A 164 közeli kontaktból tíz olyan tünetmentes volt, aki pozitívnak bizonyul a vírusspecifikus IgG-re és/vagy IgM-re.
Tanulmányunk bemutatta, hogy a MERS-CoV-fertőzést igazoló kritériumok alkalmazhatók a legtöbb COVID19-beteg esetében is. Mindazonáltal egyes betegeknél ezen kritériumok teljesítéséhez az első szérumminta lehető leghamarabb történő begyűjtése szükséges, mivel ezen betegek 12,2%-ánál (5/41) már a tünetek kezdete után 7 napon belül elérte a platót az IgG-titer (Bővített adatok, 6. ábra). Azoknál a betegeknél, akiknél nem történt mintavétel az ideális időablakban, a szerológiai vizsgálatok ismétlésére volna szükség a SARS-CoV-2-fertőzésre adott ellenyanyagválasz megerősítésére.
A tanulmányunknak van néhány korlátja. Először is, nem teszteltük a mintákat a vírusneutralizációra, ezáltal nem ismerjük az kimutatott IgG-ellenanyagok neutralizációs aktivitását. Másodszor, a súlyos vagy kritikus állapotú betegek kisszámú mintája miatt nehéz meghatározni az ellenanyagválasz és a klinikai lefolyás közötti összefüggést.
Az RT-PCR-alapú virális RNS-kimutatás érzékeny, és hatékonyan igazolhatja a korai SARS-CoV-2-fertőzést (8). Az adataink azt jelzik, hogy a COVID19-ben a vírusspecifikus ellenanyagok kimutatása fontos lehet (1) a nukleinsav-kimutatás kiegészítéseként, a negatív RT-PCR eredményű gyanús esetek diagnózisánál, valamint (2) a közeli kontaktok tünetmentes fertőzésének kiszűrésére. A COVID19-gyanús esetek lehető leghamarabbi megerősítése szerológiai vizsgálatok segítségével csökkentheti a kitettségi kockázatot az ismételt mintavételeknél, és ezáltal értékes RT-PCR-tesztek takaríthatók meg. A kisléptékű szűrésünkben hét olyan esetben, amikor negatív volt a nukleinsav-alapú eredmény és nem jelentkeztek tünetek, pozitívnak bizonyult az IgG és/vagy az IgM. Ez rávilágít a szerológiai vizsgálat fontosságára, hogy pontosabb becsléseket adhassunk a COVID19-világjárvány kiterjedéséről.
Módszerek
Vizsgálati terv
Ebbe a keresztmetszeti vizsgálatba összesen 285 COVID19-beteget vontunk be három kijelölt csungkingi kórházból. Csungking egy tartományi jogú város Hupej tartománnyal szomszédosan, amely a COVID19-járvány kiindulópontja volt. A Csungkingi Városi Népi Önkormányzat ezt a három kórházat – Chongqing Three Gorges Central Hospital (csungkingi három szurdok központi kórházat, TGH), a Yongchuan Hospital Affiliated to Chongqing Medical University (csungkingi orvosi egyetem (CQMU) jungcsuani társkórházát, YCH) és a Chongqing Public Health Medical Center (csungkingi közegészségügyi orvosi központot, CQPHMC) – jelölte ki, hogy a három területről betegeket vonjanak be a vizsgálatba. Minden vizsgálatba bevont beteg igazoltan SARS-CoV-2-fertőzött volt az orr- és garatváladék-mintából végzett RT-PCR-teszt szerint. A vizsgálatba bevont betegek mediánéletkora 47 év volt (IQR: 34–56 év), és az 55,4%-uk férfi. Közülük 250 betegnek volt epidemiológiai előzménye, míg 262 páciensnek világos emléke volt a tünetek kezdetéről, és 70 betegnek több szérummintája állt rendelkezésre. Összesen 363 szérummintát vontunk be a vizsgálatba olyan betegektől, akiknél egyértelmű volt a tünetek kezdete. A 285 beteg közül 39 volt súlyos vagy kritikus állapotban az újfajta koronavírusos tüdőgyulladás diagnosztizálásának és kezelésének protokollja (7. próbaverzió) alapján, amelyet a National Health Commission és a State Administration of Traditional Chinese Medicine (a kínai nemzeti egészségügyi bizottság és a hagyományos kínai orvoslás állami adminisztrációja) adott ki. A kohorsz nyomon követéséhez az YCH-n kezelt 63 betegtől 3 naponta vettek szérummintát 2020. február 8-tól a kórházból való elbocsátásig. Annak elemzésére, hogy a WHO által a MERS-CoV igazolására ajánlott szerológiai kritériumok megfelelők-e a COVID19 diagnosztizálására, két bevonási kritériumot jelöltünk meg a betegek szűrésére: (1) az első szérummintavétel a betegség tüneteinek megjelenése utáni első héten belül, vagy (2) az első szérummintavétel legalább 7 nappal a betegség tüneteinek megjelenését követően, de negatív IgG-vel. Az 1. kritériumnak harmincnégy beteg, a 2.-nak hét beteg felelt meg.
A COVID19 diagnózisában a szerológiai vizsgálatok potenciáljának kiértékelésére a Wanzhou People’s Hospital (vancsoui népkórház, Csungking, Kína) 52 COVID19-gyanús betegét vontunk be, akiknek légzőszervi tüneteik vagy kóros tüdőképük volt, de negatív lett az RT–PCR-eredményük legalább két egymást követő teszten. A Bővített adatok 7. ábrája szerint a megjelölt időben szérummintákat vettünk, és teszteltük a SARS-CoV-2 elleni antitesteket.
Szerológiai vizsgálatot végeztünk a 164 személyből álló közeli kontaktok klaszterében, akiket a helyi járványvédelmi és betegségmegelőzési központ azonosított (Vancsou, Csungking). Ebben a kontakthálózatban első generációs betegeknek minősítettük azt a házaspárt, akik Vuhan városából utaztak vissza, és akik 2020. február 4-én igazoltan SARS-CoV-2-fertőzöttek voltak. A kohorszban minden egyéb eset ennek a párnak a közeli (közvetlen vagy közvetett) kontaktja volt a 2020. január 20. és február 6. közötti időszakban. Március 1-jén szérummintát vettünk ettől a 164 pácienstől az ellenanyagtesztekre.
Definíciók
Az epidemiológiai előzményekkel rendelkező betegeket az alábbiak szerint határoztuk meg: Vuhani lakosok; nemrégiben jártak Vuhanban (a tünetek kezdete előtti 30 napban); helyi lakos, aki kapcsolatban állt igazolt esetekkel. A szerokonverziót úgy határozzuk meg, hogy egymást követő mintákban a SARS-CoV-2-vel szembeni IgG és IgM teszteredményei negatívból pozitívra váltottak. Az ellenanyagszinteket a mért kemilumineszcens értékek és a küszöbérték hányadosaként határoztuk meg (abszorbancia/küszöbérték, S/CO): az S/CO > 1 értéket pozitívnak minősítettük, az S/CO ≤ 1 értéket pedig negatívnak.
A SARS-CoV-2 elleni IgG és IgM kimutatása
A SARS-CoV-2 elleni IgG és IgM szintjének mérésére szérummintákat gyűjtöttünk a betegektől. Minden szérummintát 56°C-on inaktiváltunk 30 percig és –20 °C-on tároltunk a tesztelés előtt. A plazmamintákban a SARS-CoV-2 elleni IgG-t és IgM-et a Bioscience Co. által szállított MCLIA kittel teszteltük (jóváhagyta a kínai National Medical Products Administration; jóváhagyási szám: 20203400183(IgG) és 20203400182(IgM)), a gyártói útmutató alapján. Az IgG és az IgM kimutatására szolgáló MCLIA vizsgálatot a duplaellenanyag-szendvics (double-antibody sandwich) immunpróba alapján fejlesztették ki. A nukleoproteint és a SARS-CoV-2 tüskefehérjéjéből származó peptidet tartalmazó rekombináns antigéneket összekapcsoltuk FITC-vel, és immobilizáltuk az anti-FITC ellenanyaghoz konjugált mágneses részecskékre. Alkalikus foszfatázhoz konjugált antihumán IgG-/IgM-ellenanyagot alkalmaztunk kimutatási ellenanyagként. A teszteket automatizált mágneses kemilumineszcens analizátorral végeztük (Axceed 260, Bioscience) a gyártói utasításoknak megfelelően. Minden tesztre szigorú biológiai biztonsági körülmények között került sor. Az antitesttitereket szérummintánként egyszer teszteltük. Az ellenanyagszinteket a mért kemilumineszcens értékek és a küszöbérték hányadosaként határoztuk meg (S/CO). Ennek a tesztnek a küszöbértékét a hatásfokmérő karakterisztikagörbékkel határoztuk meg. Az ábrákon jelzett ellenanyagszintek számítása a következőképp történt: log2(S/CO + 1).
A SARS-CoV-2-re specifikus IgG/IgM-et kimutató módszer teljesítményének értékelése
Az MCLIA kitek pontosságát és reprodukálhatóságát először a National Institutes for Food and Drug Control (Amerikai Nemzeti Élelmiszerügyi és Gyógyszerészeti Hatóság) értékelte ki. Továbbá a COVID19-betegek 30 olyan szérummintáját is teszteltük, amelyek eltérő IgG- (0,43–187,82) és IgM-titereket (0,26–24,02) mutattak. Minden egyes mintát három független kísérletben vizsgáltunk, és a variációs együttható (CV) segítségével értékeltük a vizsgálat pontosságát. Végül 46 COVID19-betegtől származó szérumot vizsgáltunk meg a SARS-CoV-2-specifikus IgG- vagy IgM-antitestek különböző gyártási tételeibe tartozó diagnosztikai kitjeivel; a reprodukálhatóságot a két tétel tapasztalatai alapján számítottuk ki.
A SARS-CoV és a SARS-CoV-2 antigénjeinek keresztreakivitása
Két rekombináns SARS-CoV nukleokapszid (N) fehérje két különböző forrásból (Sino Biological, cat. no. 40143-V08B; Biorbyt, cat. no. orb82478), a SARS-CoV tüskefehérjéjének rekombináns S1 alegysége (Sino Biological, cat. no. 40150-V08B1) és a SARS-CoV-2 saját készítésű rekombináns N-proteinje kemilumineszcens enzim-immunvizsgálatban (CLEIA) került felhasználásra. A lemez bevonására alkalmazott antigének koncentrációja 0,5 μg/ml volt. Az alkalikus foszfatázhoz konjugált kecske antihumán IgG-antitest hígítása 1:2500 volt. COVID19-betegek öt szérummintáját és egészséges kontrollok öt szérummintáját (1:50 arányban) hígítottuk és CLEIA módszerrel teszteltük. Az ellenanyagnak egy mintában az antigénhez kötődési képességét relatív lumineszcencia egységekkel mértük.
Statisztikai elemzések
A folytonos változók mediánként kerültek meghatározásra (IQR), és összehasonlítottuk a Mann–Whitney U-próbával. A kategorikus változókat számban fejeztük ki (%) és a Fisher-féle egzakt próbával hasonlítottuk össze. A P < 0,05 értéket tekintettük statisztikailag szignifikánsnak. A statisztikai elemzéseket a 3.6.0 verziószámú R-szoftverrel végeztük.
Etikai jóváhagyás
A vizsgálatot a Ethics Commission of Chongqing Medical University (csungkingi orvosi egyetem etikai bizottsága) hagyta jóvá (hiv. sz. 2020003). A kijelölt kórház Etikai Bizottsága eltekintett az újonnan megjelenő fertőző betegségek esetében az írásos beleegyező nyilatkozattól.
A jelentés összefoglalása
A kutatás menetével kapcsolatos további információk a jelen cikkhez csatolt Nature Research Reporting Summaryben találhatók.
Az adatok elérhetősége
Ennek a tanulmánynak a nyers adatai a Kiegészítő Adatsorban (Supplementary Dataset) találhatók. További háttéradatok kérésre a levelező szerzőktől szerezhetők be. A nyers és az elemzett adatokra és anyagokra vonatkozó minden kérést áttekintenek a levelező szerzők annak biztosítására, hogy a kérelemre érvényes-e bármilyen szellemi tulajdon vagy titoktartási kötelezettség. Az 1. ábra forrásadatai és a Bővített adatok 1. és 5. ábrája online elérhetők.
Irodalom
1. Corman, V. M. et al. Viral shedding and antibody response in 37 patients with Middle East respiratory syndrome coronavirus infection. Clin. Infect. Dis. 62, 477–483 (2016).
2. Li, G., Chen, X. & Xu, A. Profile of specific antibodies to the SARS-associated coronavirus. N. Engl. J. Med. 349, 508–509 (2003).
3. Hsueh, P. R., Huang, L. M., Chen, P. J., Kao, C. L. & Yang, P. C. Chronological evolution of IgM, IgA, IgG and neutralisation antibodies after infection with SARS-associated coronavirus. Clin. Microbiol. Infect. 10, 1062–1066 (2004).
4. Park, W. B. et al. Kinetics of serologic responses to MERS coronavirus infection in humans, South Korea. Emerg. Infect. Dis. 21, 2186–2189 (2015).
5. Drosten, C. et al. Transmission of MERS-coronavirus in household contacts. N. Engl. J. Med. 371, 828–835 (2014).
6. Meyer, B., Drosten, C. & Muller, M. A. Serological assays for emerging coronaviruses: challenges and pitfalls. Virus Res. 194, 175–183 (2014).
7. Tang, Y. W., Schmitz, J. E., Persing, D. H. & Stratton, C. W. The laboratory diagnosis of COVID-19 infection: current issues and challenges. J. Clin. Microbiol. https://doi.org/10.1128/JCM.00512-20 (2020).
8. Zou, L. et al. SARS-CoV-2 viral load in upper respiratory specimens of infected patients. N. Engl. J. Med. 382, 1177–1179 (2020).
Köszönetnyilvánítás
Köszönjük C.-Y. Yangnak és L.Y. Kwannak a kézirat kritikai áttekintését. Ezt a munkát az Emergency Project from the Science & Technology Commission of Chongqing, valamint a Major National S&T Program (a csungkingi tudományos és technológiai bizottság vészhelyzeti projektje és a legnagyobb nemzeti K&T programja) támogatta (2017ZX10202203 és 2017ZX10302201).
