Eredeti cikk dátuma: 2020. március 28.
Eredeti cikk címe: Hydroxychloroquine-Azithromycin and COVID-19
Eredeti cikk szerzői: Philippe Gautret, Jean-Christophe Lagier, Philippe Parola, Van Thuan Hoang, Line Meddeb, Jacques Sevestre, Morgane Mailhe, Barbara Doudier, Camille Aubry, Sophie Amrane, Piseth Seng, Marie Hocquart, Julie Finance, Vera Esteves Vieira, Hervé Tissot Dupont, Stéphane Honoré, Andreas Stein, Matthieu Million, Phillipe colson, Bernard La Scola, Véronque Veit, Alexis Jacquier, Jean-Claude Deharo, Michel Drancourt, Pierre Edouard Fournier, Jean-Marc Rolain, Philippe Brouqui, Didier Raoult
Eredeti cikk elérhetősége: https://www.mediterranee-infection.com/hydroxychloroquine-and-azithromycin-as-a-treatment-of-covid-19/
Eredeti cikk státusza:
Fordító(k): Kozák Eszter
Lektor(ok): dr. Gampe Nóra
Nyelvi lektor(ok):
Szerkesztő(k): Novák Zsuzsanna
Figyelem! Az oldalon megjelenő cikkek esetenként politikai jellegű megnyilvánulásokat is tartalmazhatnak. Ezek nem tekinthetők a fordítócsoport politikai állásfoglalásának, kizárólag az eredeti cikk írójának véleményét tükrözik. Fordítócsoportunk szigorúan politikamentes, a cikkekben esetlegesen fellelhető politikai tartalommal kapcsolatosan semmiféle felelősséget nem vállal, diskurzust, vitát, bizonyítást vagy cáfolatot nem tesz közzé.
Az oldalon található információk nem helyettesítik a szakemberrel történő személyes konzultációt és kivizsgálást, ezért kérjük, minden esetben forduljon szakorvoshoz!
Hidroxiklorokin és azitromicin kombinált kezelés klinikai és mikrobiológiai hatása 80 COVID betegen, minimum 6 nap követéssel: megfigyeléses vizsgálat.
Hatékony kezelésre van szükség a COVID19 gyógyítására, és a vírushordozás időtartamának csökkentésére. A hidroxiklorokin és aztiromicin kezelés hatékonyságát 80 fekvőbetegen vizsgálva javulást tapasztatunk minden beteg esetében, kivéve egy 86 éves beteget, aki elhunyt, illetve egy 74 éves beteget, akit továbbra is intenzív osztályon kezelnek. Az orrgarat váladék vírustartalmát qPCR-rel vizsgálva a vírustartalom gyors csökkenését tapasztaltuk, a betegek 83%-a negatív volt a 7. napon, és 93%-a negatív volt a 8. napon. A vírustenyésztés a betegek 97,5%-ában negatív volt az 5. napon. Ez lehetővé tette a betegek korai elbocsátását a fertőző osztályról, az átlagos tartózkodási idő 5 napra csökkent. Azt gondoljuk, más kutatócsoportnak is vizsgálniuk kellene ezt a költséghatékony terápiás lehetőséget, ami gátolja a betegség terjedését és lehetővé teszi hogy kezeljük a betegeket mielőtt súlyos és visszafordíthatatlan légzőszervikomplikációk alakulnának ki.
Kulcsszavak
COVID19, SARS-CoV-2, hidroxiklorokin, azitromicin, PCR, tenyésztés
Bevezetés
Az új típusú koronavírus (SARS-CoV-2) okozta COVID19 megbetegedés először 2019. december végén a kínai Wuhan városában jelent meg, ahonnan rohamosan terjedt el a világ számos országában [1,2]. A járványt a WHO pandémiává nyilvánította 2020. március 12-én [3]. Egy kínai tanulmány szerint az esetek 80%-a csak enyhébb tünetekkel jár, és az összesített halálozás körülbelül 2,3%, de ez az arány az idősebbeknél jóval magasabb: a 70-79 éves korcsoportban 8%, a 80 év felettiek esetében pedig a 14%-ot is elérheti [4].
Mindazonáltal a feltehetően jelentős számú tünetmentes hordozó miatt ez a becslés valószínűleg túlzó. Példaként véve a Diamond Princess óceánjáró hajó fedélzetén kitört járványt, a halálozási ráta 1,4%-os volt [5]. Franciaország jelenleg a megbetegedések ugrásszerű növekedésével néz szembe, ezen cikk írásának idejében (2020.03.26) több, mint 25 000 diagnosztizált esettel [5].
A hatékony terápia megtalálása mind a betegek gyógyítása, mind a járvány további terjedésének megakadályozása szempontjából rendkívül fontos. A COVID19 kezelésében ígéretes stratégia a már használatban lévő régi hatóanyagok kipróbálása antivirális szerekként, mert ezeknél már vannak ismereteink a mellékhatásokról, a biztonságos dózisról és a más gyógyszerekkel való esetleges interakciókról [6,7].
Három in vitro tanulmány bizonyította, a klorokin-foszfát képes a SARS-CoV-2 szaporodását gátolni [8,9], és két másik igazolta ugyanezt a hidroxiklorokin-szulfát esetében [8-10]. Más tanulmányok arra mutattak rá, hogy meglévő hatóanyagok alkalmazásának kiterjesztésével (ún. repurposing felhasználás) a COVID19 kezelésében hasznos gyógyszereket azonosíthatunk, mint például a klorokin, a hidroxiklorokin és az azitromicin illetve a cukorbetegség kezelésében használt metformin, az angiotenzin receptor blokkoló zartánok vagy sztatinok, mint például a szimvasztatin [11].
Emellett a klorokin hatékonysága klinikailag is bizonyított kínai COVID19 betegek kezelésében, ahol csökkentette a lázat, javította a CT eredményeket, és késleltette a betegség progresszióját [12-14]. Ennek hatására a kínai szakértők ajánlása első helyen tartalmazza a napi kétszer 500 mg dózisban, 10 napon át adott klorokin kezelést az enyhe, középsúlyos és súlyos COVID19 megbetegedések kezelésére [15].
Egy kisebb COVID19 betegcsoporton végzett előzetes klinikai kísérletben kimutattuk, hogy a hidroxiklorokinnal kezelt (600mg/nap, n=20 beteg) csoportban szignifikánsan csökkent a vírushordozás a vizsgálat kezdetétől számított 6. napon: az orrgaratváladékot PCR-rel tesztelve a kezelt betegek 70%-a bizonyult negatívnak, míg a kezeletlen kontroll betegeknél (n=16) ez az arány csak 12,5% volt [16].
Emellett a hidroxiklorokint kapó 20 beteg közül 6-an azitromicin kezelést is kaptak 5 napig (a bakteriális felülfertőződés megelőzésére), ezen betegek mindegyike (100%) virológiai szempontból gyógyultnak volt tekinthető a 6. napon. Ez az arány az azitromicin kezelést nem kapó 14 betegnél 57,1% volt [16].
Ezzel szemben egy 30 COVID19 betegen végzett kínai tanulmány, ahol 15 beteg kapott 5 napon át 400 mg dózisú kezelést, nem mutatott ki jelentős javulást a 15 kontrollhoz viszonyítva a 7. napi garatváladék minták vírus RNS-tartalmában. Mindazonáltal ezek a betegek többféle kezelést, köztük antivirális szereket is kaptak [17].
Egy friss kínai tanulmány kimutatta, hogy a vírusürítés átlagos időtartama 20,0 nap (IQR 17.0–24.0) volt a túlélő betegek esetében, azokban pedig, akik nem élték túl a betegséget, a SARS-CoV-2 a halálukig kimutatható volt. A vírusürítés legrövidebb megfigyelt időtartama 8 nap volt, a leghosszabb pedig 37 [18]. Ennek alapján a kezelés a COVID19 betegekben lehetővé tenné a korai gyógyulást, és a vírusürítés időtartamának csökkentése segítheti a fertőzés terjedésének megakadályozását.
Ebben a tanulmányban a legalább 3 napon át adott hidroxiklorokin és azitromicin kombinált kezelés hatását mutatjuk be, 3 fő végpont szempontjából: i) klinikai eredmények, ii) PCR-rel és vírustenyésztéssel kimutatott fertőzőképesség, iii) fertőző osztályon való tartózkodás időtartama.
Módszerek
Kísérleti elrendezés és résztvevők
A fenti vizsgálat a marseilles-i University Hospital Institute Méditerranée Infection koordinálásával történt. A résztvevők a fertőző osztályunkra került, orrgarat váladék mintából PCR-rel igazolt SARS-CoV-2 RNS pozitív betegek voltak.
Fontos megjegyezni, hogy az előző cikkünkben [16] leírt 6 beteg, akiknek az állapotát 6 napig követtük, szintén bekerült ebbe a tanulmányba, hosszabb követési idővel.
Klinikai klasszifikáció és követés
A felvételkor a betegeket két csoportba osztottuk: i) felső légúti fertőzéses tüneteket mutatók (rhinitis és/vagy pharyngitis) és/vagy enyhe láz és izomfájdalom, és ii) alsó légúti fertőzéses tüneteket (bronchitis, pneumonia) mutatók. A tünetek jelentkezésétől a kórházi felvételig, illetve a tünetek jelentkezésétől a kezelés megkezdéséig eltelt időt dokumentáltuk. A súlyos lefolyású COVID19 ismert kockázati tényezőit, úgy mint idősebb kor, rák, kardiovaszkuláris betegségek, magas vérnyomás, cukorbetegség [4] illetve COPD, elhízás és bármilyen típusú immunszuppresszív kezelés, szintén dokumentáltuk.
A COVID19 betegek national early warning score (NEWS) értékét a felvételkor és a követési időszak alatt is rögzítették. Az értéket a következő paraméterek alapján számoltuk: kor, légzési ráta, oxigén szaturáció, testhőmérséklet, szisztolés vérnyomás, pulzusszám, és eszmélet szintje) [19].
A klinikai állapot romlására a COVID19 betegeknél három kockázati kategóriát határoztunk meg: alacsony kockázat (NEWS 0-4), közepes kockázat (NEWS 5-6) és magas kockázat (NEWS ≥7).
Az oxigénterápia szükségességét, az intenzív osztályra kerülést, a halálozást és a fertőző osztályon való tartózkodás hosszát rögzítettük.
Mellkas CT
A betegekről a felvételkor vagy röviddel azután alacsony dózisú mellkas CT felvételt (LDCT) készítettünk, ugyanazzal a CT készülékkel (Revolution EVO – GE Healthcare, WI, USA). Minden felvételt tapasztalt radiológusok elemeztek és osztályozták annak alapján, hogy pneumonia valószínűsíthető-e. A pneumoniát akkor tekintették valószínűnek, ha a felvételen perifériás multifokális tejüveg homály (retikulációval vagy anélkül), vagy alveoláris konszolidáció vagy „crazy paving” mintázat volt látható.
PCR vizsgálat
A vizsgálathoz az orrgaratváladék mintákat néhány kivételtől eltekintve minden betegtől naponta gyűjtötték a kórházból való hazabocsátásig. Néhány hazabocsátott beteg esetében további mintavételek is történtek járóbeteg ellátásban.
A SARS-CoV-2 RNS kimutatása real-time reverz transzkripciós PCR-rel történt, az envelope (E) protein génjét [20] célzó hidrolízises próbával, a korábbiakban leírtaknak megfelelően [20,21]. A negatívnak tekintett minták esetében a meghatározott ciklus küszöbérték (Ct) ≥35 volt.
Víruskultúra
A vírusok tenyésztése random alapon kiválasztott betegekből történt. Az orrgaratváladékból vett mintáknál a gyűjtőfolyadék 500 μL-ét 0.22-μm pórusátmérőjű centrifuga szűrőn (Merck millipore, Darmstadt, Germany) szűrtük, majd ezekkel 96-lyukú sejttenyésztő mikroplate 4 lyukában növesztett Vero E6 sejteket (ATCC CRL-1586) fertőztünk. A sejteket Minimum Essential Medium (MEM) médiumban neveltük, 4% FCS és 1% glutaminnal kiegészítve. 4000 g centrifugálást követően a plate-eket 37°C hőmérsékleten inkubáltuk, és minden nap megfigyeltük az esetleges citopatogén hatást. A vírus detektálása a felülúszóban SU5000 SEM (Hitachi) segítségével történt, amit specifikus RT-PCR vizsgálattal erősítettünk meg.
COVID19 kezelés
Azoknál a betegeknél, ahol ez nem volt kontraindikált (lásd az 1. sz. kiegészítő dokumentumot), felajánlottuk a szájon át 10 napig adott napi 3x 200 mg hidroxiklorokin-szulfát kezelést, amit kiegészítettünk 500 mg azitromicinnel az első napon, majd napi 250 mg dózisban az azt követő 4 napon. Azoknál a betegeknél, ahol pneumoniát diagnosztizáltunk és 5 feletti NEWS érték mellett ezt széles spektrumú antibiotikum (ceftriaxon) kezeléssel egészítettük ki.
Minden beteg esetében végeztünk 12 elvezetéses elektrokardiográfiát (EKG) a kezelés megkezdése előtt, és a kezelés kezdete utáni második napon. Minden EKG felvételt tapasztalt kardiológusok értékeltek ki. A kezelést nem kezdtük meg, illetve leállítottuk, ha a QTc (Bazett korrekciós formula szerint) meghaladta az 500ms-ot. A 460 és 500 ms közé eső QTc értékek esetén a kockázat-előny mérlegelése alapján egyedileg döntöttünk a kezelésről.
A kezelést nem kezdtük meg ha az EKG örökletes ioncsatorna rendellenességre utalt és a kockázat-előny viszonyokat egyedileg mérlegeltük, ha más rendellenességet (például patológiás Q hullám, balkamra hipertrófia vagy bal Tawara szár blokk, BTSzB) találtunk.
Emellett, a kezelés időtartamára leállítottuk minden gyógyszer alkalmazását, ami a QT intervallumot nyújtja. Szükség esetén tüneti kezelést, beleérte oxigén terápiát alkalmaztunk. A felvételt követően a szérum ionszinteket – különös tekintettel a káliumra – folyamatosan ellenőriztük, és szükség szerint a rutin laborparamétereket is ellenőriztük.
Elbocsátási kritériumok
Az elbocsátási kritériumok a tanulmány időtartama alatt változtak. Eleinte minden olyan beteget hazabocsátottak, akinek az orrgaratváladék mintájában a PCR vizsgálat nem mutatott ki vírust (Ct ≥35) két egymást követő mintában.
Március 18 után elég volt egy negatív (Ct≥34) PCR teszteredmény ahhoz, hogy a betegek hazamehessenek vagy a kezelésüket más osztályon folytassák. Végül, mivel nagy szükség volt arra, hogy az újonnan érkező kezeletlen betegeket el tudjuk helyezni az osztályon, a bennfekvő kezelt betegek közül a <34 PCR eredményű betegek körül azok, akiknek a klinikai állapota megfelelő volt, és a kezeléssel kapcsolatos előírásokat betartották, szintén hazamehettek. Amikor erre lehetőség volt, a további követésüket más osztályokon vagy járóbeteg ellátás keretében folytattuk.
Fertőzőképesség kritériumai
A PCR teszteken <34 küszöbérték érték alatti betegeket feltételezhetően fertőzőnek tekintettük, arra a tanulmányra támaszkodva (https://www.mediterranee-infection.com/pre-prints-ihu/) ami szerint ilyen körülmények között a tenyésztés jellemzően negatív eredményt ad. Pozitív tenyésztés esetén a betegeket fertőzőnek tekintettük.
Kimenetel
Az elsődleges végpontok i) súlyos klinikai lefolyás, ami szükségessé tette az oxigénterápiát vagy az intenzív osztályra való áthelyezést legalább három nap kezelés után, és ii) fertőzőképesség PCR vagy vírustenyésztés segítségével meghatározva, és iii) fertőző osztályon való tartózkodás időtartama.
Statisztika
A vírustenyésztés sikerességi arányának szórását statisztikailag úgy határoztuk meg, mint a teljes variancia Ct értékkel magyarázható hányada és a kapcsolat akkor minősült megfelelőnek, ha a determinációs együttható (R2) értéke 0.5 feletti volt.
A tenyésztési sikerességből sz statisztikai vizsgálata során a variancia Ct érték által megmagyarázott hányadát akkor fogatuk el megfelelő illeszkedésként, ha az R2 érték >50% volt.
Etikai nyilatkozat
A kísérleti protokollt engedélyezte a University Hospital Institute Méditerranée Infection (N°: 2020-01) etikai bizottsága. A vizsgálat a Helsinki Bizottság és annak kiegészítései által ajánlott jó klinikai gyakorlatnak megfelelően zajlott.
Eredmények
Demográfiai adatok és a betegek felvételkor felmért állapota (1. és 2. táblázat).
80 COVID19 miatt hospitalizált beteg közül 77 a Méditerranée Infection University Hospital Intézetben, 3 pedig egy ideiglenes COVID19 ellátó osztályon kapott kezelést 2020 március 3-21 között.
Az analízisbe azok a betegek is bekerültek, akik legalább három napi hidroxiklorokin és azitromicin [16] kezelést kaptak és minimum 6 napos utókövetésben részesültek. A betegek életkorának medián értéke 52 év volt (18 és 88 év között), a nők és férfiak aránya ~1:1 volt. A betegek 57,5%-ának volt legalább egy ismert COVID19 betegséget súlyosbító rizikótényezőt jelentő krónikus társbetegsége. A leggyakoribbak ezek közül a magas vérnyomás, cukorbetegség és a krónikus légzőszervi megbetegedés voltak. A tünetek jelentkezése és a kórházi felvétel között eltelt átlagos időtartam 5 nap volt, a leghosszabb tapasztalt időtartam 17 nap volt.
A betegek 53,8%-ának voltak alsó légúti fertőzéses tünetei, és 41,2%-uknak voltak felső légúti fertőzéses tünetei. Láza csak 15%-nak volt. Négyen tünetmentes hordozók voltak. A betegek túlnyomó többsége (92%) a NEWS score szempontjából alacsony kockázati csoportba tartozott, az alacsony dózisú CT felvételek szerint 53,8%-nál voltak pneumoniára utaló eltérések a mellkas CT-n. A PCR vizsgálatok átlagos Ct értéke 23,4 volt.
Hidroxiklorokin és azitromicin kombinált kezelés (2. és 3. táblázat).
A tünetek jelentkezésétől a kezelés kezdetéig eltelt átlagos idő 4,9 nap volt, a legtöbb betegnél (93,7%) a kezelést a kórházi felvétel napján vagy másnap megkezdtük. A 80-ból 79 beteg kapott napi szinten kezelést a tanulmány teljes időtartama (vagyis maximum 10 nap) alatt. Egy beteg esetében az egyébként jól tolerált kezelést le kellett állítani a 4. napon, potenciális gyógyszerkölcsönhatás miatt. A tapasztalt mellékhatások ritkák voltak és enyhék.
Klinikai lefolyás (3. táblázat)
A betegek többségénél (65/80, 81,3%) a lefolyás kedvező volt, ezeket a betegeket a tanulmány írásának időpontjában már alacsony NEWS érték mellett hazabocsátottuk (61/65, 93,8%). Csak 15%-nak volt szüksége oxigén terápiára. Három beteget átszállítottak az intenzív osztályra, közülük kettő javulást mutatott, így később visszakerült a fertőző osztályra. Egy 74 éves beteget a tanulmány írásának időpontjában továbbra is az intenzív osztályon ápolnak. Végül egy 86 éves beteg, akit nem szállítottak át az intenzív osztályra a fertőző osztályon elhunyt (1. kiegészítő táblázat).
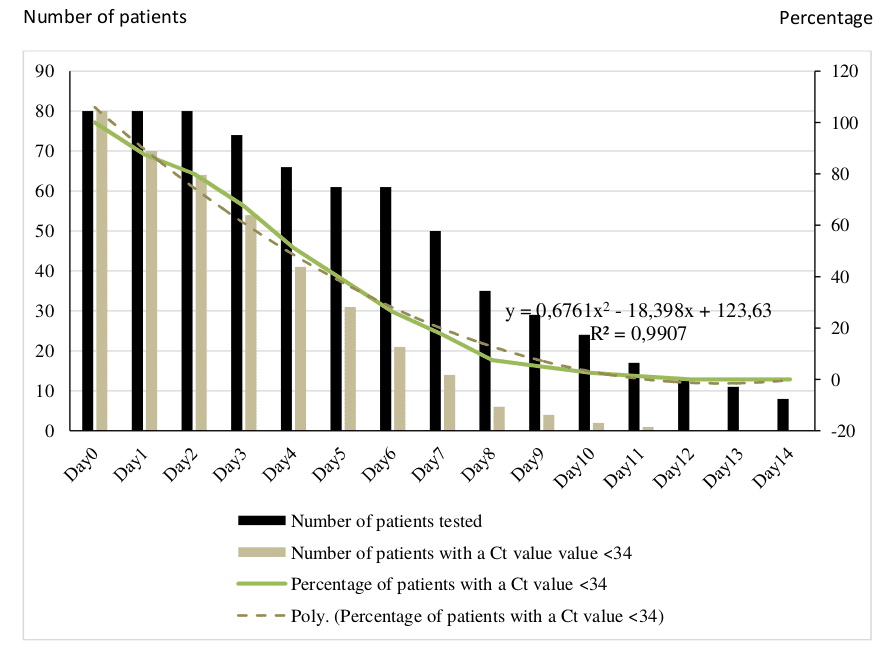
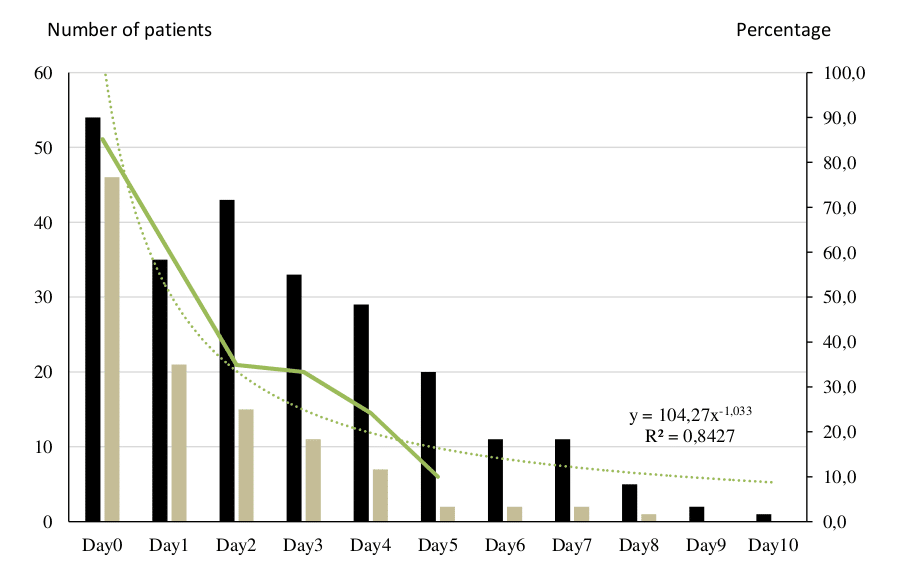
PCR Ct érték és tenyésztés által meghatározott fertőzőképesség (1. és 2. ábra)
A qPCR az orrgaratváladék mintákban a vírusmennyiség gyors csökkenését mutatta, a betegek 83%-a volt negatív a 7. napon, illetve 93%-a a 8. napon. A feltételezhetően fertőző (PCR Ct érték <34) betegek aránya folyamatosan csökkent, és a 12. napon elérte a nullát (1. ábra). Jelentős csökkenés volt megfigyelhető a kezelés hatodik napja után. 10 nap után két beteg maradt feltételezhetően fertőző, 32-es, illetve 29-es Ct értékkel. A 34 feletti Ct értéket mutató betegek aránya idővel szignifikánsan csökkent (R2=0,9). A betegek légúti mintáiból végzett vírustenyésztés 97,5%-ban negatív volt az 5. napon. A (pozitív kultúrával igazolt) fertőző betegek száma a kezelés 3. napja után csökkent (2. ábra). A kezelés 5. napja után már csak 2 beteg volt fertőző. A 8. napon a két beteg közül már csak az egyik volt fertőző, és a 9. napon már ez a beteg sem. A tenyésztéssel igazolt negatív betegek aránya idővel szignifikánsan csökkent! (Szerk. megj.: ez valószínűleg elírás, és a betegek aránya növekedett. A vezető kutatót megkerestük e-mailben és amint választ kapunk frissítjük a cikket.) (R2=0,8).
A fertőző osztályon való tartózkodás időtartama
Az osztályról elbocsátott 65 beteg esetében a kezelés megkezdése és a hazabocsátás között eltelt átlagos idő 4,1 nap volt, a kórházi tartózkodás átlagos időtartama 4,6 nap.
Diszkusszió
A COVID19 két nagy nehézség elé állítja az orvosokat.
Az első a betegek kezelése. Ennek kontextusában fontos a tüdőgyulladás súlyosbodásának megakadályozása, ami általában a 10. nap körül következik be, és ARDS kialakulásához vezet, aminek a prognózisa idős korban a kiváltó októl függetlenül mindig rossz. A terápia elsődleges célja tehát a közepes vagy súlyos fertőzések korai fázisban történő kezelése, mielőtt a betegek visszafordíthatatlanul súlyos állapotba kerülnek.
Azitromicinnel kombinált hidroxiklorokin kezeléssel minden betegnél javulást értünk el, kivéve egy 86 éves beteget, aki nagyon előrehaladott betegséggel jelentkezett, és az állapotának romlását nem tudtuk megállítani.
A 80 fős kohortban minden más beteg esetében a kombinált kezelés klinikailag hatékonynak bizonyult a betegség irodalomban leírt természetes lefolyásához viszonyítva. Egy 191 beteget tartalmazó kínai kohort esetében, ahol a betegek 95%-a kapott antibiotikum kezelést és 21% kapott lopinavir és ritonavir kezelést, a láz átlagos időtartama 12 nap volt, a köhögésé 19 a túlélő betegek esetében, 28%-os halálozási arány (CFR) mellett [18].
A hidroxiklorokin és azitromicin kezelt betegeink esetében a kedvező lefolyás a PCR-rel meghatározott virális RNS szintek gyors csökkenésével járt, ami még gyorsabbnak bizonyult, ha tenyésztéssel vizsgáltuk. Fontos ezeket összevetni az irodalmi adatokkal, amik szerint a vírus RNS ürítése a betegek nagy részénél akár három héten át magas maradhat specifikus kezelés alkalmazásának hiányában [18,22]. Extrém esetekben az akár több mint egy hónapot is jelenthet.
Egy 76 kínai COVID19 betegen végzett tanulmány szerint a nagyobb vírus RNS tartalom a súlyosabb lefolyású betegség kialakulásával mutat korrelációt [23]. Továbbá egy 16 kínai bennfekvő betegen végzett tanulmány szerint a tünetek elmúlása után átlagosan 2,5 napig (maximum 8 napig) a betegek 50%-ában továbbra is kimutatható volt a vírus RNS [24].
Tehát a virális RNS termelés csökkenése a kezelés sikerességét alátámasztó egyik elem. Tudomásunk szerint a kezelés hatékonyságának vizsgálatára vírustenyésztést ebben a tanulmányban alkalmaztunk először. A pozitív kultúrák számának esése 48 nap után (Szerk. megj.: ez valószínűleg elírás, és 48 óraután. A vezető kutatót megkerestük e-mailben és amint választ kapunk frissítjük a cikket.)lenyűgöző hatékonyságot jelent, bár az esetek kis részében néhány beteg tenyésztése továbbra is pozitív maradt.
A második kihívás a járvány gyors terjedése a populációban a fertőző személyek közvetítésével. A vírus hordozásának megszüntetése az emberi rezervoárban nemrég felismert prioritás [25]. Ennek elérésében nagy jelentősége lehet annak, hogy a hidroxiklorokin és azitromicin kezelés hatására a betegek légzőszervi mintái gyorsan negatívvá váltak.
Emellett ezzel a tanulmánnyal párhuzamosan kutatócsoportunk in vitro SARS-CoV-2 fertőzött sejteken vizsgálta a hidroxiklorokin és azitromicin kezelés hatását, jelentős szinergizmust igazolva a két hatóanyag között a betegek szervezetében feltételezhetően jelenlevő koncentrációk esetében (https://www.mediterranee-infection.com/pre-prints-ihu2/). Ennélfogva a kezelés direkt terápiás hatása mellett segíthet a járvány kontrollálásában a vírusürítés – kezelés hiányában jellemzően több héten át tartó – időtartamának csökkentésével. Intézetünkben, ahol 75 különálló szobával rendelkezünk az erősen fertőző betegek elkülönítésére, jelenleg1/3-os fluktuációs aránnyal, ami lehetővé teszi, hogy nagy számú fertőző beteget fogadjunk, akiket korán haza tudunk bocsátani.
A klorokin és hidroxiklorokin igen jól ismert gyógyszerek, amiket emberek milliárdjainak írtak már fel. Mivel bizonyos alapbetegségek esetében előfordulhatnak szívkomplikációk ezeknek a gyógyszereknek az adásakor egyes források szerint, hasznos lehet az EKG vizsgálat a kezelést megelőzően vagy annak kezdetekor [26]. Ez a probléma megoldható az ilyen szempontból magasabb kockázatú betegek befektetésével és rendszeres EKG monitorozásával, hogy korán észrevegyük és kezelhessük ezeket a ritka, de lehetséges kardiológiai mellékhatásokat.
Az azitromicin a légzőszervi megbetegedések esetében leggyakrabban felírt antibiotikum, egy friss (2010) tanulmány szerint 8-ból 1 járóbeteg ellátásban kezelt amerikai betegnek írtak már fel [27]. Ennek megfelelően valószínűleg már több egy milliárd alkalommal írtak fel azitromicint világszerte a felfedezése óta. A toxicitás tehát egyik hatóanyag esetében sem lehet jelentős probléma. A két hatóanyag kombinációjának toxicitásával kapcsolatban anekdotikus beszámolók vannak, de tudomásunk szerint ezt máig nem sikerült bizonyítani.
Összegezve, bizonyítjuk a hidroxiklorokin és azitromicin kombinációjának hatékonyságát a COVID19 kezelésében és a fertőzés terjedésének korai megállításában. Mivel égető szükség van a betegség kezelésére hatékony és biztonságos gyógyszerekkel, és mivel a hidroxiklorokin és azitromicin kezelés költségei elhanyagolhatóak, azt gondoljuk, hogy más kutatócsoportoknak is sürgősen vizsgálniuk kellene ezt a terápiás stratégiát a járvány megállítására és a betegek kezelésére még a súlyos és visszafordíthatatlan légzőszervi komplikációk kialakulása előtt.
Kiegészítő dokumentumok
A hidroxiklorokin és azitromicin kezelés kontraindikációi
Hidroxiklorokin
A kezelés abszolút kontraindikációi a hidroxiklorokinra illetve klorokinra, amino-4 kinolinokra, amodiakinra, meflokinra, glafeninre, floktafeninre, antrafeninre való túlérzékenység, retinopátia, 6 év alatti kor, szoptatás, citalopram, eszcitalopram, hidroxizin, domperidon és piperakin szedése, az aritmia és torsades de pointes (TdP) megnövekedett kockázata miatt.
Relatív kontraindikációt jelent a hepatikus porfíria, laktóz túlérzékenység, galaktóz anyagcsere zavarai, laktáz enzim hiány, illetve emésztőrendszeri malabszorpció / intolerancia szindróma a segédanyagként tartalmazott laktóz miatt.
Azitromicin
A kezelés abszolút kontraindikációi az ismert túlérzékenység az azitromicinre, eritromicinre, klarithromicinre, dirithromicinre, josamicinre, midekamicinre, diacetátra, roxitromicinre, telitromicinre, makrolidokra, ketolidokra, everolimuszra, pimekrolimuszra, sirolimuszra, temsirolimuszra, fidaxomicinre, mogyoróolajra és szójára.
Szintén kontraindikációt jelentenek a álhártyáskolitisz, anafilaxiás sokk, komoly bőrtünetek, akut exantémás pusztulózis, DRESS szindróma, komoly májelégtelenség, kolhicin, cizaprid, dihidroergotaim és ergotamin szedése.
Használata nem ajánlott kolesztázis esetén és olyanok számára akik bromokriptint, kabergolint, lizuridot vagy pergolidot szednek. Szedése nem ajánlott a tejcukorra való túlérzékenység, a galaktóz anyagcsere zavara, laktáz hiány illetve emésztőrendszeri malabszorpció / intolerancia szindróma esetén a segédanyagként tartalmazott laktóz miatt.
Forrás:
Theriaque: independent-drug database for good use of drugs by health practitioners. Husson MC. Ann Pharm Fr. 2008 Nov-Dec;66(5-6):268-77. 5. http://www.theriaque.org
Köszönetnyilvánítás
Megköszünjük Christine Zandotti, Laetitia Ninove, Céline Boschi, Véronique Filosa, Marion Bechet, Ahmed Yacine Belkhir, Sébastien Cortaredona, Patrick Peretti-Watel, Pierre Verger, Yolande Obadia, és a klinikusok, technikusok és mentősök segítségét a kórházakban és a laboratóriumokban ebben a nehéz helyzetben.
Támogatás forrása
A kísérlet az Institut Hospitalo-Universitaire (IHU) Méditerranée Infection, a francia nemzeti kutatási alap “Befektetés a jövőbe” (Investissements d’avenir) programja, és az Agence Nationale de la Recherche (ANR, fr: National Agency for Research), ANR-10-IAHU-03) Région Provence Alpes Côte d’Azur és az Európai FEDER PRIMI támogatásával valósult meg.
Hivatkozásjegyzék
[1] Lai CC, Shih TP, Ko WC, Tang HJ, Hsueh PR. Severe acute respiratory syndrome coronavirus 2 (SARS-CoV-2) and coronavirus disease-2019 (COVID-19): The epidemic and the challenges. Int J Antimicrob Agents. 2020 Mar;55(3):105924.
[2] Zhu N, Zhang D, Wang W, Li X, Yang B, Song J, et al. A Novel Coronavirus from Patients with Pneumonia in China, 2019. N Engl J Med. 2020 Feb 20;382(8):727-33.
[3] WHO Director-General’s opening remarks at the media briefing on COVID-19 – 11 March 2020. [https://www.who.int/dg/speeches/detail/who-director-general-s-opening-remarks-at-the-media-briefing-on-covid-19—11-march-2020] 2020.Ref Type: Internet Communication
[4] Wu Z, McGoogan JM. Characteristics of and Important Lessons From the Coronavirus Disease 2019 (COVID-19) Outbreak in China: Summary of a Report of 72314 Cases From the Chinese Center for Disease Control and Prevention. JAMA 2020 Feb 24.
[5] Coronavirus COVID-19 Global Cases by the Center for Systems Science and Engineering (CSSE) at Johns Hopkins University (JHU) (accessed on March, 26 th 2020 from https://gisanddata.maps.arcgis.com/apps/opsdashboard/index.html#/bda7594740fd40299423467b48e9ecf6
[6] Colson P, Rolain JM, Raoult D. Chloroquine for the 2019 novel coronavirus SARS-CoV-2. Int J Antimicrob Agents. 2020 Feb 15;105923.
[7] Colson P, Rolain JM, Lagier JC, Brouqui P, Raoult D. Chloroquine and hydroxychloroquine as available weapons to fight COVID-19. Int J Antimicrob Agents. 2020 Mar 4;105932.
[8] Yao X, Ye F, Zhang M, Cui C, Huang B, Niu P, et al. In Vitro Antiviral Activity and Projection of Optimized Dosing Design of Hydroxychloroquine for the Treatment of Severe Acute Respiratory Syndrome Coronavirus 2 (SARS-CoV-2). Clin Infect Dis. 2020 Mar 9.
[9] Liu J, Cao R, Xu M, Wang X, Zhang H, Hu H, et al. Hydroxychloroquine, a less toxic derivative of chloroquine, is effective in inhibiting SARS-CoV-2 infection in vitro. Cell Discov. 2020;6:16.
[10] Wang M, Cao R, Zhang L, Yang X, Liu J, Xu M, et al. Remdesivir and chloroquine effectively inhibit the recently emerged novel coronavirus (2019-nCoV) in vitro. CellRes. 2020 Mar;30(3):269-71.
[11] Nabirothckin S, Peluffo AE, Bouaziz J, Cohen D. Focusing on the Unfolded Protein Response and Autophagy Related Pathways to Reposition Common Approved Drugs against COVID-19. Preprints 2020;doi: 10.20944/preprints202003.0302.v1.
[12] Gao J, Tian Z, Yang X. Breakthrough: Chloroquine phosphate has shown apparent efficacy in treatment of COVID-19 associated pneumonia in clinical studies. Biosci Trends. 2020 Feb 19.
[13] Chinese Clinical Trial Registry. http://www.chictr.org.cn/ searchproj.aspx?title. Ref Type: Internet Communication
[14] Zhou D, Dai SM, Tong Q. COVID-19: a recommendation to examine the effect of hydroxychloroquine in preventing infection and progression. J Antimicrob Chemother. 2020 Mar 20.
[15] Multicenter collaboration group of Department of Science and Technology of Guangdong Province and Health Commission of Guangdong Province for chloroquine in the treatment of novel coronavirus pneumonia. [Expert consensus on chloroquine phosphate for the treatment of novel coronavirus pneumonia]. Zhonghua Jie He He Hu Xi Za Zhi 2020 Mar 12;43(3):185-8. doi: 10.3760/cma.j.issn.1001-0939.2020.03.009.
[16] Gautret P, Lagier JC, Parola P, Hoang VT, Meddeb L, Mailhe M, et al. Hydroxychloroquine and azithromycin as a treatment of COVID-19: results of an open-label non-randomized clinical trial. Int J Antimicrob Agents. 2020 Mar 20;105949.
[17] Chen J, Liu D, Liu L, Liu P, Xu Q, Xia L, et al. A pilot study of hydroxychloroquine in treatment of patients with common coronavirus disease-19 (COVID-19). J of Zjeijang University. 2020.
[18] Zhou F, Yu T, Du R, Fan G, Liu Y, Liu Z, et al. Clinical course and risk factors for mortality of adult inpatients with COVID-19 in Wuhan, China: a retrospective cohort study. Lancet. 2020 Mar 11.
[19] Liao X, Wang B, Kang Y. Novel coronavirus infection during the 2019-2020 epidemic: preparing intensive care units-the experience in Sichuan Province, China. Intensive Care Med. 2020 Feb;46(2):357-60.
[20] Corman VM, Landt O, Kaiser M, Molenkamp R, Meijer A, Chu DKW, et al. Detection of 2019 novel coronavirus (2019-nCoV) by real-time RT-PCR. Euro Surveill 2020. Jan;25(3).
[21] Amrane S, Tissot-Dupont H, Doudier B, Eldin C, Hocquart M, Mailhe M, et al. Rapidviral diagnosis and ambulatory management of suspected COVID-19 cases presenting at the infections diseases referral hospital in Marseille, France, -January 31st to March 1st, 2020: A respiratory virus snapshot. Travel Med Infect Dis. 2020;in press.
[22] To KK, Tsang OT, Leung WS, Tam AR, Wu TC, Lung DC, et al. Temporal profiles of viral load in posterior oropharyngeal saliva samples and serum antibody responses during infection by SARS-CoV-2: an observational cohort study. The Lancet. 2020;Published on line March 23,2020.
[23] Liu Y, Yan LM, Wan L, Xiang TX, Le A, Liu JM, et al. Viral dynamics in mild and severe cases of COVID-19. Lancet Infect Dis. 2020 Mar 19.
[24] Chang, Mo G, Yuan X, Tao Y, Peng X, Wang F, et al. Time Kinetics of Viral Clearance and Resolution of Symptoms in Novel Coronavirus Infection. Am J Respir Crit Care Med. 2020 Mar 23.
[25] Mitja O, Clotet B. Use of antiviral drugs to reduce COVID-19 transmission. Lancet Glob Health. 2020 Mar 19.
[26] Chatre C, Roubille F, Vernhet H, Jorgensen C, Pers YM. Cardiac Complications Attributed to Chloroquine and Hydroxychloroquine: A Systematic Review of the Literature. Drug Saf. 2018 Oct;41(10):919-31.
[27] Hicks LA, Taylor TH, Jr., Hunkler RJ. U.S. outpatient antibiotic prescribing, 2010. N Engl J Med. 2013 Apr 11;368(15):1461-2.
