Eredeti cikk dátuma: 2020. március 13.
Eredeti cikk címe: The convalescent sera option for containing COVID-19
Eredeti cikk szerzői: Arturo Casadevall, Liise-anne Pirofski
Eredeti cikk elérhetősége: https://www.jci.org/articles/view/138003
Eredeti cikk státusza:
Fordító(k): Legindi Zoltán
Lektor(ok): dr. Benedek-Kováts Emese
Nyelvi lektor(ok): Rét Anna
Szerkesztő(k): Novák Zsuzsanna
Figyelem! Az oldalon megjelenő cikkek esetenként politikai jellegű megnyilvánulásokat is tartalmazhatnak. Ezek nem tekinthetők a fordítócsoport politikai állásfoglalásának, kizárólag az eredeti cikk írójának véleményét tükrözik. Fordítócsoportunk szigorúan politikamentes, a cikkekben esetlegesen fellelhető politikai tartalommal kapcsolatosan semmiféle felelősséget nem vállal, diskurzust, vitát, bizonyítást vagy cáfolatot nem tesz közzé.
Az oldalon található információk nem helyettesítik a szakemberrel történő személyes konzultációt és kivizsgálást, ezért kérjük, minden esetben forduljon szakorvoshoz!
2020 elejétől az emberiség a súlyos heveny légúti tünetegyüttest okozó koronavírus 2 (SARS-CoV-2) pandémiával néz szembe. A SARS-CoV-2 okozza a COVID19 rövidítéssel jelölt koronavírus-betegséget. A cikk írása idején a SARS-CoV-2 számos országban terjed, és emberek milliárdjait érintő pandémia kialakulásával fenyeget. Ez a vírus egy új humán patogénnek tűnik. Jelenleg a SARS-CoV-2 ellen nem áll rendelkezésre vakcina, monoklonális antitest vagy gyógyszer, habár sok van már fejlesztés alatt, és néhány rövid időn belül hozzáférhetővé válhat. Nézőpontunk szerint a humán rekonvaleszcens plazma a COVID19 megelőzésének és kezelésének egy olyan módja, amely gyorsan elérhető, ha van elegendő gyógyult egyén, aki képes immunglobulin-tartalmú plazmát adományozni.
Passzív antitest-terápia
A passzív antitest-terápia (passzív immunizáció/vakcináció) egy bizonyos ágens elleni antitestek adását jelenti az erre fogékony személyeknek avval a céllal, hogy az adott ágens által okozott fertőző betegséget megakadályozza vagy kezelje. Ezzel szemben az aktív vakcináció az immunválasz kialakulását igényli, ami időbe telik, és a vakcinát kapó egyéntől függően változik. Tehát a passzív immunizáció az egyetlen módszer, hogy azonnali immunitást biztosítsunk a fogékony személyeknek. A passzív antitest-terápia története egészen az 1890-es évekig nyúlik vissza, és ez volt az egyetlen eszköz bizonyos fertőző betegségek gyógyítására, mielőtt az 1940-es években kifejlesztették az antimikrobiális terápiát (1, 2). A korábbi koronavírusos járványokkal, mint a SARS-CoV-1, kapcsolatban szerzett tapasztalataink azt mutatják, hogy az ilyen rekonvaleszcens szérumok tartalmazzák az adott vírusra ható neutralizáló antitesteket (3).
A SARS-CoV-2 esetében a feltételezett hatásmechanizmus, amellyel a passzív antitest-terápia elősegíti a védelmet, az a vírus semlegesítése. Habár egyéb mechanizmusok is lehetségesek, mint például az antitestfüggő celluláris citotoxicitás és/vagy a fagocitózis. A SARS-CoV-2 elleni antitestek lehetséges forrása a COVID19-ből felépült személyektől származó rekonvaleszcens plazma, a monoklonális antitestek vagy bizonyos állati gazdaszervezetben kialakuló készítmények, mint például a genetikailag módosított tehenek által termelt humán antitestek (4). Bár sokféle készítmény fejlesztése van folyamatban vagy kezdődik el hamarosan, jelenleg az egyetlen, azonnali alkalmazásra rendelkezésre álló antitesttípus az, amelyik a humán rekonvaleszcens plazmában található (1. ábra). Ahogy egyre több ember kapja el a COVID19-et és gyógyul meg belőle, a lehetséges donorok száma is folyamatosan növekszik.
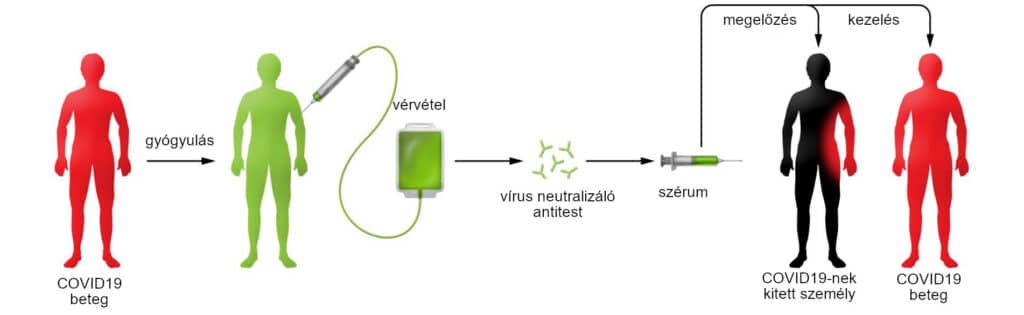
A rekonvaleszcens plazma COVID19 elleni alkalmazásának sematikus ábrázolása. A COVID19-ben szenvedő, majd abból felépülő személytől vért vesznek, majd azt vírus neutralizáló antitestekre tesztelik. Kiválasztják azokat, akiknél a neutralizáló antitestek titere magas, majd a tőlük nyert szérumot a fertőzés megakadályozására beadhatják megelőzésként a magas kockázatú egyéneknek, mint például az alapbetegségekkel rendelkező veszélyeztetett személyeknek, az egészségügyi dolgozóknak és azoknak, akik igazolt COVID19-esetekkel állnak kapcsolatban. Ezen kívül a tünetek és a halálozás csökkentése érdekében a rekonvaleszcens plazma potenciálisan alkalmazható a klinikailag beteg egyéneknél. Ezeknek a módszereknek a hatékonysága ismeretlen, de a korábbi tapasztalatok azt sugallják, hogy a rekonvaleszcens plazma sokkal hatásosabb lehet a megelőzésben, mint a már kialakult betegség kezelésében.
A passzív antitest-terápia általános elve szerint is sokkal hatékonyabb egy betegség megelőzésére, mint a kezelésére. Ha terápiaként alkalmazzák, az antitest akkor a leghatékonyabb, ha nem sokkal a tünetek jelentkezését követően adják be. A hatásosság időbeli eltérésének oka még nem teljesen ismert, de azt tükrözheti, hogy a bevitt antitest a kezdeti inokulum neutralizálásával hat, amely jóval kevesebb, mint a már kialakult betegségnél (5). Egy másik magyarázat szerint az antitest a gyulladásos válaszreakciót módosítja, ami könnyebben érhető el az immunválasz kezdetekor, vagyis abban a szakaszban, amely még tünetmentes lehet (6). Például a passzív immunizáció akkor volt a leghatásosabb a Pneumococcus okozta tüdőgyulladás esetén, ha röviddel a tünetek kialakulását követően alkalmazták, ám nem volt eredménye, ha az antitestet a betegség harmadik napját követően adták be (7).
Ahhoz, hogy a passzív antitest-terápia hatásos legyen, megfelelő mennyiségű antitest bejuttatása szükséges. Ha fogékony személy kapja, az antitest keringeni kezd a vérben, eljut a szövetekbe és biztosítja a fertőzéssel szembeni védelmet. Az antitest mennyiségétől és összetételétől függően a beadott immunglobulin által kialakított védettség hetekig, akár hónapokig tarthat.
Múltbéli előfordulások
A huszadik század elején a rekonvaleszcens plazmát alkalmazták többek között a következő vírusok okozta járványok megakadályozására: járványos gyermekbénulás (8), kanyaró (9, 10), mumpsz (11) és influenza (12). Az 1918-as H1N1 influenza (spanyolnátha) pandémia során a rekonvaleszcens plazma használatát vizsgáló, 1703 beteget érintő nyolc tanulmány retrospektív metaanalízise azt mutatta, hogy a szérumot kapók halálozási aránya kisebb volt (13). Bár a rekonvaleszcens plazma hatásossága vírusonként és tanulmányonként eltérő volt, mégis akkoriban arra jutottak, hogy a beavatkozás hasznos volt, és számos járvány során alkalmazták. Érdemes megjegyezni, hogy korábban a rekonvaleszcens szérumot sok esetben használták anélkül, hogy mérték volna az antitesttitereket, vagy ismerték volna a vírus szerotípusát, illetve olyan klinikai vizsgálatok során, amelyek nem felelnek meg a randomizáció vagy vak mintavétel modern kritériumainak.
A közelmúltban a rekonvaleszcens szérumot vírusok okozta járványok idején alkalmazták. A 2009-2010-es H1N1 influenzavírus pandémia idején az aferézis útján szerzett rekonvaleszcens plazma antitest készítményeket intenzív ápolást igénylő, súlyos H1N1/09-fertőzésben szenvedő személyek kezelésére használták (14). A szérummal kezelt pácienseknél csökkent a légzőszervi vírusterhelés, a plazma citokinválasz és a halálozás (14). A 2013. évi nyugat-afrikai ebolajárvány idején szintén rekonvaleszcens szérumot használtak. A Sierra Leonéban folytatott kis méretű, nem-randomizált vizsgálat jelentősen hosszabb túlélést mutatott azoknál, akiket rekonvaleszcens teljes vérrel kezeltek, mint azoknál, akik a standard kezelést kapták (15). Az a két páciens, akit az Egyesült Államokba szállítottak, majd rekonvaleszcens plazma és egy kísérleti gyógyszer kombinációjával kezeltek, szintén életben maradt (16). Anekdotikus bizonyítékok szerint a H5N1 (17, 18) és a H7N9 (19) madárinfluenza-járványok kitörése során a rekonvaleszcens plazma alkalmazása hatásos volt, és valamennyi kezelt túlélte a betegséget.
Habár minden vírusbetegség és járvány eltérő, ezek a tapasztalatok bíztatók és hasznosak, amikor az emberiség szembenéz a COVID19-járvánnyal.
A rekonvaleszcens plazma koronavírus okozta betegségek elleni alkalmazásának tapasztalatai
A XXI. században két másik, magas halálozással járó koronavírus-járvány fordult elő, a 2003-as SARS1 és a 2012-es közel-keleti légzőszervi tünetegyüttes (MERS). A SARS1-járványt megfékezték, viszont a MERS Közel-Keleten endémiává alakult, és Dél-Koreában másodlagosan nagy járványt okozott. Mindkét járvány során a magas halálozás és a hatékony terápiák hiánya vezetett a rekonvaleszcens plazma alkalmazásához. A legnagyobb volumenű tanulmány 80 hongkongi SARS-beteg kezelését vizsgálta (20). A 14. napot megelőzően kezelt betegek prognózisa javult, azaz a 22. nap előtt elbocsátották őket a kórházból, ami egybecseng azzal a felvetéssel, hogy minél előbb alkalmazzák, annál valószínűbb a hatássosága (20). Ráadásul javult a prognózis azoknál, akik a koronavírusra PCR-pozitívok és szeronegatívok voltak a terápia idején (20). Van néhány anekdotikus információ is arról, hogy súlyos betegeknél alkalmazták a rekonvaleszcens szérumot. Tajvanban három SARS-beteget kezeltek 500 ml rekonvaleszcens szérummal, aminek eredményeképpen csökkent a plazma vírustitere, és mindannyian életben maradtak (21). Dél-Koreában három MERS-beteg kapott rekonvaleszcens szérumot, de csak kettőnek volt neutralizáló antitest a szérumában (22). Ez utóbbi kihangsúlyozza a rekonvaleszcens plazma használatával kapcsolatos kihívást, nevezetesen hogy néhány vírusbetegségből felépültnél fordulhat elő, hogy nem magasak a neutralizáló antitesttiterek (23). Ezzel összecseng, hogy SARS-betegektől származó 99 rekonvaleszcens plazma vizsgálata kimutatta, hogy 87 tartalmazott neutralizáló antitestet, amelyeknél a titerek geometrikus középértéke 1:61 volt (3). Ez azt tételezi fel, hogy az antitestmennyiség idővel csökken és/vagy néhány beteg magas titerű választ produkál. Az is elképzelhető, hogy nem-neutralizáló antitestek termelődnek, és azok járulnak hozzá a védelemhez és a gyógyuláshoz, ahogy ezt már más vírusbetegségek esetén is leírták (24–26). Vannak arra vonatkozó beszámolók, hogy Kínában a jelenlegi járvány során a rekonvaleszcens szérumot alkalmazták COVID19-betegek kezelésére (27). Habár a kínai járvány kapcsán kevés részlet áll rendelkezésre, illetve kis számú beteget érintő tanulmányokat publikáltak, az elérhető információk szerint a rekonvaleszcens plazma adagolása csökkentette a vírusterhelést és biztonságos volt.
Kockázatok és előnyök
A COVID19 rekonvaleszcens plazma alkalmazható akár a fertőzés megelőzésére, akár a betegség kezelésére. A megelőzés során a rekonvaleszcens plazma alkalmazása azért előnyös, mert megakadályozza a fertőzést és a betegség követezményes kialakulását a magas kockázatú esetekben, például az alapbetegségekkel rendelkező veszélyeztetett személyeknél, az egészségügyi dolgozóknál és azoknál, akik igazolt COVID19-betegekkel állnak kapcsolatban. A betegség megelőzésére már a klinikai gyakorlatban használják az antitest bevitelét. Például a hepatitis-B és a veszettség vírusnak kitett betegeket az adott betegségnek megfelelően hepatitis-B immunglobulinnal (HBIG) és humán rabies immunglobulinnal (HRIG) kezelik. Mindezek mellett a veszélyeztetett csecsemőknél a súlyos, légúti óriássejtes vírus (RSV) okozta betegség megelőzésére passzív immunizációt alkalmaznak. Mostanáig magas RSV neutralizáló antitesttiterrel rendelkező donoroktól származó mintákból előállított poliklonális hiperimmun-globulint (RSV-IG) használtak, de ezeket a készítményeket jelenleg már a palivizumab, humanizált egér monoklonális antitest helyettesíti. Gyógyászati céllal alkalmazva a rekonvaleszcens plazma beadható azoknak, akik klinikailag betegek, a tünetek és a halálozás csökkentésére. Ezeknek az eljárásoknak a hatásossága nem igazolható kontrollált klinikai vizsgálatok nélkül. Az antitest alkalmazásával kapcsolatos korábbi tapasztalatok alapján feltételezhető, hogy az sokkal hatékonyabb lehet a megelőzésben, mint a már kialakult betegség kezelésében (12).
A rekonvaleszcens plazma adásának kockázata két kategóriába sorolható: az ismertbe és a teoretikusba. Az ismert kockázatok a vér alkotóelemeinek adásával függenek össze. Ide tartoznak például a gondatlanság miatt más betegséget okozó ágenssel történő fertőzés, valamint a plazma alkotóelemei által kiváltott reakciók, mint a szérumbetegség és más immunológiai reakciók. Modern transzfuziológiai technikákkal szűrik a vérrel terjedő kórokozókat, illetve ellenőrzik a donor és a recipiens vércsoportjának kompatibilitását. Ennek köszönhetően az ismert fertőző ágensek gondatlan átvitelének vagy a transzfúziós reakciók kiváltásának kockázata meglehetősen alacsony. Ám nagy valószínűséggel olyan egyének kapnák terápiás céllal a rekonvaleszcens szérumot, akiknél már tüdőbetegség áll fenn, ezért a plazmainfúzió adásakor nagyobb a transzfúzióval összefüggő akut tüdőkárosodás (TRALI) kockázata (28), amit figyelembe kell venni a kockázatok és előnyök értékelése során. A teoretikus kockázat magában foglalja az ellenanyagfüggő fertőzésfokozódás (ADE) jelenségét. Az ADE számos vírusbetegség esetén jelentkezhet, ahol bizonyos antitestek jelenlétében a betegség súlyosbodhat. A koronavírusok kapcsán az ADE számos mechanizmusát leírták, és teoretikusan feltételezhető, hogy az egyik koronavírus elleni antitestek fokozhatják egy másik vírustörzs általi fertőzést (29). Az ADE kockázata a SARS-CoV-2 esetén kísérleti úton előrejelezhető, ugyanúgy, mint ahogy a MERS esetén is javasolt (29). Mivel a COVID19-járvány során olyan rekonvaleszcens plazma alkalmazását javasolják, amelyben magas az azonos vírus, a SARS-CoV-2 elleni neutralizáló antitestek titere, az ADE kialakulása nem valószínű. A rekonvaleszcens plazma SARS1- és MERS- (30) betegeken történő alkalmazásáról rendelkezésre álló bizonyítékok, valamint a 245 Covid19-betegen történő alkalmazás anekdotikus bizonyítékai (27) azt mutatják, hogy biztonságos. Mindazonáltal figyelmet és elővigyázatosságot igényel a rekonvaleszcens plazma klinikai vizsgálatai során a fertőzésfokozódás jeleinek felismerése.
Egy másik elméleti kockázat az, hogy a SARS-CoV-2-nek kitett embereknél az antitestek alkalmazása az immunválasz gyengítése révén akadályozza a megbetegedést, ám ennek következményeként fogékonyabbá is teszi az egyént a későbbi újrafertőződésre. E tekintetben azt jelentették, hogy az RSV-védőoltást megelőző passzív immunizáció gyengítette a humorális immunitást, a cellulárist azonban nem (31). Ez az eredmény klinikai vizsgálat részeként ellenőrizhető azáltal, hogy mérik az immunválaszát azoknak, akiket a betegség megelőzése érdekében rekonvaleszcens szérummal kezeltek. Amennyiben ez a kockázat bizonyítást nyer, ezek a személyek megkaphatják a COVID19 elleni védőoltást, amint az elérhetővé válik.
Ha elfogadjuk, hogy a múltbéli és jelenlegi anekdotikus adatok szerint a rekonvaleszcens plazma alkalmazása a koronavírus-fertőzésben biztonságos, a COVID19-cel összefüggő, különösen az időseket és a veszélyeztetett személyeket érintő magas halálozás azt sugallja, hogy annak használata a magas rizikójúaknál vagy a betegség korai szakaszában előnyösebb, mint amennyi kockázatot jelent. Mindazonáltal minden olyan esetben, amikor felmerül a rekonvaleszcens plazma adásának lehetősége, az egyéni változók értékelése érdekében kockázat-előny elemzés szükséges. A közelmúltban hivatkoztak ezekre a megfontolásokra, amikor eldöntötték, hogy alkalmazzák a monoklonális antitesteket az ebola vírusbetegség kezelésében (32).
Bevezetés és javasolt alkalmazás
A rekonvaleszcens plazma COVID19 esetében történő alkalmazásának bevezetéséhez a következő hat feltételnek kell teljesülnie: (i) rendelkezésre állnak olyan donorok, akik felépültek a betegségből és rekonvaleszcens plazmát tudnak adni; (ii) biztosítva vannak a plazma feldolgozásának eszközei; (iii) elérhetők a megfelelő tesztek, beleértve a szerológiai teszteket, amelyekkel kimutatható a SARS-CoV-2 a plazmában, valamint azok, amelyek mérik a vírus neutralizációját; (iv) biztosított a vizsgálatok végrehajtásához szükséges laboratóriumi háttér; (v) ki vannak dolgozva a megelőzési és kezelési protokollok, amelyek ideális esetben tartalmazzák a randomizált klinikai vizsgálatokat, melyek értékelik a beavatkozások hatásosságát és mérik az immunválaszt; (vi) megfelel a szabályozásoknak, beleértve az intézményi felügyeleti szervek jóváhagyását, amely az egyes helyeken eltérő lehet. Ideális esetben a rekonvaleszcens plazma alkalmazása multicentrikus, randomizált vizsgálati protokollt követ, és egy koordináló központtal rendelkezik. Ezek közül minden egyes feltételnek teljesülnie kell a COVID19-cel érintett fejlett területeken. Legalább egy gyógyszergyár, a Takeda fokozott erővel állítja elő a COVID19-betegek rekonvaleszcens szérumából a SARS-CoV-2 elleni készítményeket (33). A neutralizáló antitestek magas titerét tartalmazó, rendkívül nagy tisztaságú SARS-CoV-2 elleni készítmények előállítása kívánatosabb, mint a rekonvaleszcens plazma, mivel azok biztonságosabbak és nagyobb az aktivitásuk. Sajnos ezek a készítmények még hónapokig nem állnak rendelkezésre, ugyanakkor a helyben előállított rekonvaleszcens plazma sokkal hamarabb elérhető.
Feltételezzük, hogy amint a jogszabályokban előírt szükséges engedélyek rendelkezésre állnak, a COVID19-ből felépült személyek felkereshetők, hogy aferézis úján vért adjanak a szérumkészítmények előállításához vagy antitest izolálásához. Klinikailag értékelik a COVID19-ből történő gyógyulást, és ezeknek a személyeknek a megfelelő vírus-nukleinsav-szűrés alapján a vérükben is SARS-CoV-2-mentességet kell mutatniuk. Az adományozott vérkészítményeket a jelenlegi transzfuziológiai eljárásoknak megfelelően szűrik fertőző ágensekre, és egyénileg vizsgálják a plazmában a specifikus antitesttartalmat, illetve a SARS-CoV-2-vel szembeni neutralizáló hatást. A szükséges mennyiség és a rekonvaleszcens plazma neutralizáló hatásának függvényében ezek összegyűjthetők vagy alkalmazhatók önmagukban is. A klinikai felhasználásra szánt készítményeket a kórokozók gyengítése céljából kezelik. Jelenleg még nem tudjuk, hogy a megelőzésként alkalmazott passzív immunizáció esetén a fogékony személyekben mekkora a hatásos antitesttiter, ezért ennek a paraméternek a meghatározása része a tanulmányoknak. Úgyszintén nem tudjuk azt sem, hogy mekkora dózis lenne terápiásan hatásos. Azt azonban tudjuk, hogy a kanyaró és a mumpsz megakadályozására felhasznált rekonvaleszcens plazma mennyisége 10–40 cm3 (10-40 ml) volt (10, 11). Ezzel szemben amikor a rekonvaleszcens plazmát súlyos, spanyolnáthában szenvedő katonáknál alkalmazták, a beadott mennyiség többszáz milliliter volt (34). Ezek a régi vizsgálatok hatásosságot mutattak annak ellenére, hogy a rekonvaleszcens plazmát a neutralizáló titerek ismerete nélkül alkalmazták. Ezen tapasztalatok azt sugallják, hogy még az antitestek kis mennyisége is képes megakadályozni és/vagy kezelni a fertőzést. Tehát feltételezhetjük, hogy a hatásos megelőző dózis jóval kisebb, mint a terápiás. Ez logikusnak tűnik, hiszen a fertőző inokulum feltehetőleg jóval kisebb, mint a vírusterhelés egy súlyos betegség során.
A COVID19 rekonvaleszcens plazma alkalmazható a korai tüneteket mutató betegek kezelésére, illetve a fertőzésnek kitettek esetében a betegség megelőzésére. Manapság az ápolónők, az orvosok és a mentősök kapcsolatba kerülnek az ismert COVID19-betegekkel, és néhányuk, akiknél kialakult a betegség, karanténba kerül, ami az egészségügy összeomlását okozhatja. Feltételezhető, hogy a rekonvaleszcens plazma megakadályozza a SARS-CoV-2-fertőzést azoknál, akiknél alkalmazták. Amennyiben ez igazolható, azok a személyek, akik megkapják a rekonvaleszcens plazmát, elkerülhetik a karantént. Ez pedig lehetővé tenné, hogy egészségügyi dolgozóként folytassák a kritikus feladataik teljesítését. A rekonvaleszcens plazma arra is használható, hogy a COVID19-ben szenvedő családtagjaikat ápoló személyek megbetegedését megakadályozza. Egyértelmű, hogy a rekonvaleszcens plazma alkalmazása hézagpótló megoldás lehet a mostani járvány közepén. Ugyanakkor még a helyi alkalmazás is jelentős koordinációt igényel a különböző résztvevők, pl. az infektológusok, a hematológusok, a transzfuziológusok és a kórházvezetők között. Mivel a világjárvány közepén járunk, javasoljuk, hogy az intézmények fontolják meg a rekonvaleszcens plazma sürgősségi alkalmazását, és a lehető leghamarabb kezdjék meg az előkészületeket. Az időtényező nem elhanyagolható.
Köszönetnyilvánítás
Rendkívül hálásak vagyunk Shmuel Sholamnak a segítőkész megjegyzéseiért és javaslataiért. Arturo Casadevall részben az NIH HL059842, AI052733 és AI152078 támogatását élvezte. Liise-anne Pirofski részben az NIH 6R01AG045044-07, AI123654 és AI143453 támogatását élvezte.
Érdekellentétek: A szerzők kijelentik, hogy nem áll fenn összeférhetetlenség.
Copyright: © 2020, American Society for Clinical Investigation.
Szakirodalomra vonatkozó információ: J Clin Invest. 2020;130(4):1545–1548. https://doi.org/10.1172/JCI138003.
Irodalomjegyzék
- Zhang JS, et al. A serological survey on neutralizing antibody titer of SARS convalescent sera. J Med Virol. 2005;77(2):147–150.
- Beigel JH, et al. Safety and tolerability of a novel, polyclonal human anti-MERS coronavirus antibody produced from transchromosomic cattle: a phase 1 randomised, double-blind, single-dose-escalation study. Lancet Infect Dis. 2018;18(4):410–418.
- Robbins JB, Schneerson R, Szu SC. Perspective: hypothesis: serum IgG antibody is sufficient to confer protection against infectious diseases by inactivating the inoculum. J Infect Dis. 1995;171(6):1387–1398.
- Casadevall A, Pirofski LA. Antibody-mediated regulation of cellular immunity and the inflammatory response. Trends Immunol. 2003;24(9):474–478.
- Casadevall A, Scharff MD. Serum therapy revisted: animal models of infection and development of passive antibody therapy. Antimicrob Agents Chemother. 1994;38(8):1695–1702.
- Park WH. Therapeutic use of antipoliomyelitits serum in preparalytic cases of poliomyelitis. JAMA. 1932;99:1050–1053.
- Park WH, Freeman RG. The prophylactic use of measles convalescent serum. JAMA. 1926;87(8):556–558.
- Gallagher JR. Use of convalescent measles serum to control measles in a preparatory school. Am J Public Health Nations Health. 1935;25(5):595–598.
- Rambar AC. Mumps; use of convalescent serum in the treatment and prophylaxis of orchitis. Am J Dis Child. 1946;71:1–13.
- Luke TC, Casadevall A, Watowich SJ, Hoffman SL, Beigel JH, Burgess TH. Hark back: passive immunotherapy for influenza and other serious infections. Crit Care Med. 2010;38(4 suppl):e66–e73.
- Luke TC, Kilbane EM, Jackson JL, Hoffman SL. Meta-analysis: convalescent blood products for Spanish influenza pneumonia: a future H5N1 treatment? Ann Intern Med. 2006;145(8):599–609.
- Hung IF, et al. Convalescent plasma treatment reduced mortality in patients with severe pandemic influenza A (H1N1) 2009 virus infection. Clin Infect Dis. 2011;52(4):447–456.
- Sahr F, et al. Evaluation of convalescent whole blood for treating Ebola virus disease in Freetown, Sierra Leone. J Infect. 2017;74(3):302–309.
- Kraft CS, et al. The Use of TKM-100802 and convalescent plasma in 2 patients with Ebola virus disease in the United States. Clin Infect Dis. 2015;61(4):496–502.
- Kong LK, Zhou BP. Successful treatment of avian influenza with convalescent plasma. Hong Kong Med J. 2006;12(6):489.
- Zhou B, Zhong N, Guan Y. Treatment with convalescent plasma for influenza A (H5N1) infection. N Engl J Med. 2007;357(14):1450–1451.
- Wu XX, Gao HN, Wu HB, Peng XM, Ou HL, Li LJ. Successful treatment of avian-origin influenza A (H7N9) infection using convalescent plasma. Int J Infect Dis. 2015;41:3–5.
- Cheng Y, et al. Use of convalescent plasma therapy in SARS patients in Hong Kong. Eur J Clin Microbiol Infect Dis. 2005;24(1):44–46.
- Yeh KM, et al. Experience of using convalescent plasma for severe acute respiratory syndrome among healthcare workers in a Taiwan hospital. J Antimicrob Chemother. 2005;56(5):919–922.
- Ko JH, et al. Challenges of convalescent plasma infusion therapy in Middle East respiratory coronavirus infection: a single centre experience. Antivir Ther (Lond). 2018;23(7):617–622.
- Arabi YM, et al. Feasibility of using convalescent plasma immunotherapy for MERS-CoV infection, Saudi Arabia. Emerging Infect Dis. 2016;22(9):1554–1561.
- van Erp EA, Luytjes W, Ferwerda G, van Kasteren PB. Fc-mediated antibody effector functions during respiratory syncytial virus infection and disease. Front Immunol. 2019;10:548.
- Jenks JA, Goodwin ML, Permar SR. The roles of host and viral antibody fc receptors in herpes simplex virus (HSV) and human cytomegalovirus (HCMV) infections and immunity. Front Immunol. 2019;10:2110.
- Gunn BM, et al. A role for Fc function in therapeutic monoclonal antibody-mediated protection against ebola virus. Cell Host Microbe. 2018;24(2):221–233.e5.
- China puts 245 COVID-19 patients on convalescent plasma therapy. News release. Xinhua. February 28, 2020. Accessed March 10, 2020. http://www.xinhuanet.com/english/2020-02/28/c_138828177.htm.
- Gajic O, et al. Transfusion-related acute lung injury in the critically ill: prospective nested case-control study. Am J Respir Crit Care Med. 2007;176(9):886–891.
- Wan Y, et al. Molecular mechanism for antibody-dependent enhancement of coronavirus entry. J Virol. 2020;94(5):e02015-19.
- Mair-Jenkins J, et al. The effectiveness of convalescent plasma and hyperimmune immunoglobulin for the treatment of severe acute respiratory infections of viral etiology: a systematic review and exploratory meta-analysis. J Infect Dis. 2015;211(1):80–90.
- Crowe JE, Firestone CY, Murphy BR. Passively acquired antibodies suppress humoral but not cell-mediated immunity in mice immunized with live attenuated respiratory syncytial virus vaccines. J Immunol. 2001;167(7):3910–3918.
- Mulangu S, et al. A randomized, controlled trial of Ebola virus disease therapeutics. N Engl J Med. 2019;381(24):2293–2303.
- Hopkins JS. Drugmaker Takeda Is Working on Coronavirus Drug. Wall Street Journal. https://www.wsj.com/articles/drugmaker-takeda-is-working-on-coronavirus-drug-11583301660 Published March 4, 2020. Accessed March 10, 2020.
- McGuire LW, Redden WR. The use of convalescent human serum in influenza pneumonia-a preliminary report. Am J Public Health (N Y). 1918;8(10):741–744.
Verziótörténet
- 1. verzió (2020. március 13.) Elektronikus kiadvány
- 2. verzió (2020. március 13.) Metadata fix
- 3. verzió (2020. április 1.) Nyomtatás

További információk a terápiás lehetőségekről itt.
