Eredeti cikk dátuma: 2020. december 11.
Eredeti cikk címe: BNT162b2 induces SARS-CoV-2-neutralising antibodies and T cells in humans
Eredeti cikk szerzői: Karikó Katalin, Ugur Sahin, Alexander Muik, Isabel Vogler, Evelyna Derhovanessian, Lena M. Kranz, Mathias Vormehr, Jasmin Quandt, Nicole Bidmon, Alexander Ulges, Alina Baum, Kristen Pascal, Daniel Maurus, Sebastian Brachtendorf, Verena Lörks, Julian Sikorski, Peter Koch, Rolf Hilker, Dirk Becker, Ann-Kathrin Eller, Jan Grützner, Manuel Tonigold,
Eredeti cikk elérhetősége: https://www.medrxiv.org/content/10.1101/2020.12.09.20245175v1
Eredeti cikk státusza: preprint
Fordító(k): dr. Szabó Edit, Györkei Ádám
Lektor(ok): dr. Serly Julianna
Nyelvi lektor(ok): Csornainé Nagy Ágnes
Szerkesztő(k): Lehoczki-Bárány Réka, Vinkovits Mária
Figyelem! Az oldalon megjelenő cikkek esetenként politikai jellegű megnyilvánulásokat is tartalmazhatnak. Ezek nem tekinthetők a fordítócsoport politikai állásfoglalásának, kizárólag az eredeti cikk írójának véleményét tükrözik. Fordítócsoportunk szigorúan politikamentes, a cikkekben esetlegesen fellelhető politikai tartalommal kapcsolatosan semmiféle felelősséget nem vállal, diskurzust, vitát, bizonyítást vagy cáfolatot nem tesz közzé.
Az oldalon található információk nem helyettesítik a szakemberrel történő személyes konzultációt és kivizsgálást, ezért kérjük, minden esetben forduljon szakorvoshoz!
A BNT162b2, egy lipid nanorészecskével (LNP) formulázott, nukleoziddal módosított hírvivő RNS (mRNS), amely a fúzió előtti konformációban stabilizálódott súlyos akut légzőszervi tünetegyüttest okozó koronavírus 2 (SARS-CoV-2) tüskefehérjét (S) kódolja, és 95%-os hatékonyságú a 2019-es koronavírus-betegség (COVID19) megelőzésében. A közelmúltban előzetesen beszámoltunk a BNT162b2 biztonságossági és antitestválasz-adatairól egy folyamatban lévő, placebokontrollos, megfigyelő számára vak, klinikai I./II. fázisú vakcina vizsgálatban1. Bemutatjuk egy második, nem-randomizált, nyílt elrendezésű, I./II. fázisú, 19-55 éves felnőtteken végzett vizsgálat, 1-30 µg első/emlékeztető dózisú BNT162b2-vakcina beadása utáni ellenanyag- és T-sejt-válaszokat. A BNT162b2 erős antitestválaszt váltott ki, az S-kötő IgG koncentrációja meghaladta a COVID19-cel fertőzött humán konvaleszcens minta (HCS) panelben mért értékeket. A 29. napon (7 nappal az emlékeztető oltás után) a szérum SARS-CoV-2 50%-os neutralizációs geometriai átlagtitere legalább 0,3-szorosa (1 µg), és legfeljebb 3,3-szorosa (30 µg) volt a HCS-panelben mértnek. A BNT162b2-vel oltottakból származó szérum neutralizálta a sokféle SARS-CoV-2 S-variánssal rendelkező pszeudovírusokat. Ezzel egyidejűleg a legtöbb résztvevő esetében jelentősen emelkedett az S-specifikus CD8+ és az 1-es típusú segítő (TH1) CD4+ T-sejtek száma, ami nagy mennyiségű interferon-γ (IFNγ) termelésével járt együtt. Peptid MHC-multimerek alkalmazásával azonosítottuk azokat a BNT162b2 indukálta, gyakori MHC-allélokon prezentált epitópokat, amelyeket a CD8+ T-sejtek felismertek. Kimutattuk, hogy a CD8+T-sejtek korai differenciált effektormemória-fenotípusúak, és a speciális sejtpopulációk egyenként a keringő CD8+ T-sejteknek a 0,01-3%-át tették ki. Összefoglalva, a BNT162b2-vackina jól tolerálható dózisokban kombinált adaptív humorális és celluláris immunválaszt vált ki, amelyek együttesen hozzájárulhatnak a COVID19 elleni védelemhez.
MEGJEGYZÉS: Ez a nyomtatás előtti jelentés olyan új kutatásról számol be, amely egyelőre nem esett át szakértői értékelésen, és amely klinikai gyakorlatban nem használható fel.
Bevezetés
Tekintettel arra, hogy milyen jelentős hatása van a súlyos akut légzőszervi tünetegyüttest okozó koronavírus 2 (SARS-CoV-2) okozta világjárványnak az emberi társadalomra, a biztonságos és hatásos profilaktikus vakcinák gyors kifejlesztése rendkívül fontos.
A lipid nanorészecskével (LNP) formulázott hírvivő RNS (mRNS)-vakcina technológia az immunogén pontos genetikai információját juttatja el az antigénprezentáló sejtekhez, és erős immunválaszt vált ki2. A mRNS csak átmenetileg expresszálódik, nem integrálódik a genomba, és fiziológiai útvonalak révén lebomlik. A mRNS-vakcinák molekulárisan jól definiáltak, és hatékonyan szintetizálódnak a DNS-templátokról in vitro transzkripcióval, amely sejtes és állati eredetű anyagoktól mentes3–5. Az mRNS-termelés és az LNP-formulázás gyors, magasan skálázható folyamat, amely alkalmassá teszi ezt a technológiát a vakcina gyors kifejlesztésére és a járvány alatti vakcinaellátásra6–8.
A „Project Lightspeed” keretében, amelyhez a BioNTech-Pfizer COVID19 RNS-vakcina-fejlesztési program is csatlakozott, két I./II. fázisú ernyő (umbrella, többtényezős) klinikai vizsgálat folyik, az egyik Németországban (NCT04380701), a másik az USA-ban (NCT04368728), amelyekben összesen négy RNS-LNP vakcinajelöltet vizsgálnak. A közelmúltban beszámoltunk ezeknek a vizsgálatoknak az előzetes klinikai adatairól a két legelőrehaladottabb fázisban tartó BNT162b19,10 és BNT162b21 vakcinajelölt esetében. Mindegyik jelölt egy LNP-formulázott, farmakológiailag optimalizált11,12, N1-metil-pszeudouridin (m1ψ) nukleoziddal módosított mRNS (modRNS)13, amelyet intramuszkulárisan adnak be két dózisban, az emlékeztetőt az első dózishoz képest 21 nappal később. A BNT162b1 az S receptorkötő doménjének (RBD) trimerizált, szekretált változatát, míg a BNT162b2 a teljes hosszúságú, a fúzió előtti konformációban stabilizált SARS-CoV-2 S-t kódolja (P2 S)14.
A BNT162b2-t 30 µg-os, kétdózisú adagolási rendben választották ki egy folyamatban lévő, II./III. fázisú vizsgálat előrehaladása érdekében, a két I./II. fázisú vizsgálatban és az NHP-provokációs vizsgálatokban kapott összesített adatokból levont következtetések alapján1,15. A placebokontrollos, megfigyelő számára vak, az USA-ban zajló, I./II. fázisú vizsgálatban a 18–55 és 65–83 éves résztvevők BNT162b2-vel történt immunizálása legfeljebb 30 µg-os dózissal általában enyhe vagy közepesen súlyos helyi oltási reakciókkal és szisztémás eseményekkel, például fáradtsággal, fejfájással és izomfájdalommal járt1. A BNT162b2 robusztus S1-kötő immunglobulin G(IgG)-koncentrációt és SARS-CoV-2 neutralizáló titert eredményezett. A fiatalabb és idősebb felnőttektől származó szérumok neutralizáló titereinek (GMT) geometriai átlaga 50% hét nappal a második 30 µg-os BNT162b2 dózis után 3,8-szoros, illetve 1,6-szoros volt a COVID19 konvaleszcens humán szérumok paneljének GMT-jéhez képest. Az USA-ban zajló I./II. fázisú vizsgálatban közzétett eredményeket kiegészítve és kibővítve a következőkben a német vizsgálat adatait mutatjuk be (NCT04380701, EudraCT: 2020- 001038-36). Beszámolunk az 1, 10, 20 és 30 µg-os BNT162b2 első-emlékeztető oltás immunogenitásáról és biztonságosságáról a 19-55 év közötti résztvevőknél, beleértve a neutralizáló antitest GMT-it az első dózis után (kb. két hónappal az emlékeztető oltást követően) a 85. napig, és a T-sejt-válaszoknak a részletes leírását, beleértve a COVID19-vakcinával kiváltott CD8+ T-sejtek által felismert epitópok első azonosítását.
Vizsgálati elrendezés és elemzési módszerek
A 19-55 éves résztvevőket Németországban BNT162b2-vel oltották be (1. kibővített adatábra). A résztvevők átlagéletkora 40 év, 56%-uk nő volt, és mindenki a kaukázusi rasszhoz tartozott (1.kibővített adattáblázat). Dóziskohorszonként tizenkét résztvevőt jelöltek ki, akik az 1. napon 1, 10, 20 vagy 30 μg első dózist kaptak, a 22. napon pedig emlékeztető oltást (2. kibővített adattáblázat). Az 1 µg és a 10 µg-os dóziskohorszból egy-egy egyént kizártak az emlékeztető oltás előtt. Mindegyik dóziskohorszban az antitestszinteket és a vírusneutralizációs titereket 10-12 résztvevőnél értékeltük időponttal (a 85. napig, 63 nappal az emlékeztető oltás után), és a perifériás vér mononukleáris sejtjeit (PBMC) 8-10 résztvevőnél elemeztük a celluláris immunválaszra a kiinduláskor és a 29. napon (7 nappal az emlékeztető oltás után) (2. kibővített adattáblázat).
Biztonságosság és tolerálhatóság
Röviden, nem figyeltek meg súlyos nemkívánatos eseményeket (SAE) és kapcsolódó nemkívánatos események (AE-k) miatti visszalépést egyik dózisszinten sem. A helyi reakciók, elsősorban az injekció beadásának helyén fellépő fájdalom, enyhék vagy közepesen súlyosak voltak (1. és 2. súlyossági fokú), és hasonlóak voltak az első, valamint az emlékeztető dózisok után gyakoriságukban és súlyosságukban (2.a kibővített adatábra és 3.a kibővített adattáblázat). A leggyakoribb szisztémás AE-k a fáradtság, illetve ezt követően a fejfájás volt, és csak két résztvevő számolt be enyhe lázról (2.b kibővített adatábra és 3.b kibővített adattáblázat). Az átmeneti hidegrázás az emlékeztető oltás után gyakoribb volt, dózisfüggő és esetenként súlyos mértékű. Az izomfájdalom és az ízületi fájdalom is gyakoribb volt az emlékeztető után, és dózisfüggő súlyosságot mutatott. Nem voltak 4. súlyossági fokú reakciók. A reakciók általában az immunizálástól számított 24 órán belül jelentkeztek, az immunizálást követő napon tetőztek, és többnyire 2-3 napon belül megszűntek. A reakciók nem igényeltek kezelést, vagy egyszerű intézkedésekkel (pl. paracetamol) kezelhetők voltak.
A BNT162b2 oltást követően a rutin vérkép laboratóriumi értékeiben nem történt klinikailag jelentős változás. Az RNS-alapú vakcinákról szóló korábbi jelentésekkel1,9,10,16 összhangban a vér limfocitaszámának enyhe csökkenését (egyidejű neutropénia nélkül) és a C-reaktív protein (CRP) növekedését figyelték meg, ezek mind átmenetiek, dózisfüggőek és a laboratóriumi normális szinteken belül vagy azok közelében voltak (3. kibővített adatábra). Mindkét hatást az RNS-vakcinák hatásmechanizmusa farmakodinamikai markereinek tekintik: a vér limfocitaszáma átmenetileg csökken, mivel a limfociták a veleszületett immunstimulációra reagálva újra eljutnak a limfoid szövetekbe17, a CRP pedig a veleszületett immunmoduláció következményes hatása18-21.
A vakcina kiváltotta antitestválasz jellemzése
Az S1- és RBD-kötő IgG-koncentrációkat és a SARS-CoV-2 neutralizáló titereket kiinduláskor (1. nap), valamint 7 és 21 nappal a BNT162b2 első dózisa után (8. és 22. nap), és az emlékeztető oltás után a 7., a 21., a 28. és a 63. napon értékeltük (a 29., a 43. és az 50. napon; a 85. napon minden dózisszintnél, kivéve az 1 µg-ot) (1. ábra, 4. kibővített adatábra, 2. kibővített adattáblázat).
1. ábra | BNT162b2 indukálta IgG-koncentrációk és a vírusneutralizációs titerek
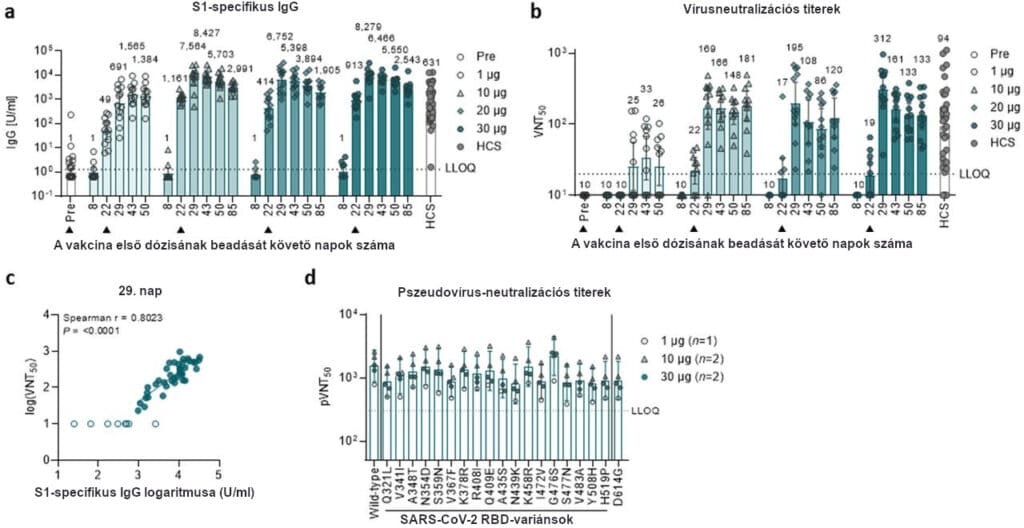
A vakcina erős antitestválaszokat váltott ki. Az első dózis után 21 nappal az S1-kötő IgG geometriai átlagkoncentrációi (GMC-k) minden dóziskohorszban növekedtek, az S1-kötő IgG GMC-k 49–1,161 U/ml tartományba estek, és csak az 1 µg-os és a 10 µg-os dózisszinttel találtunk bizonyítékot a dózisszintfüggő immunválaszra (1.a ábra). Hét nappal az emlékeztető oltás után (a 29. napon) az S1-kötő IgG GMC-k erős választ mutattak az emlékező oltásra, a 691–8,279 U/ml tartományba estek. Az antitestszintek az idő múlásával csökkentek, de az S1-hez kötődő antitest GMC-k a 85. napon (63 nappal az emlékeztető után) még mindig az 1,384–2,991 U/ml tartományba estek, és ennélfogva jóval meghaladták a SARS-CoV-2 konvaleszcens betegek szérumpaneljében megfigyelt szintet (631 U/ml). Hasonló megfigyeléseket végeztek, amikor az RBD domént használták célantigénként (4. kibővített adatábra).
A SARS-CoV-2-t 50%-ban neutralizáló geometriai átlagtiterek (GMT-k) mérsékelten, és csak a résztvevők egy részében nőttek a BNT162b2 első dózisa után (1.b ábra). Az emlékeztető dózis után hét nappal a neutralizáló GMT-k szintje lényegesen megnőtt 169-re, 195-re vagy 312-re, a 10, a 20 vagy a 30 µg-os BNT162b2-vel immunizált résztvevőkben. Az 1 µg-os dózisszint csak minimális neutralizációs választ váltott ki (GMT 25 az emlékeztető oltás után hét nappal). A 43. napon (21 nappal az emlékeztető oltást követően) a BNT162b2 10 és 30 µg közötti dózisszintjeivel oltott résztvevők vírusneutralizációs GMT-i 108 és 166 között voltak. Fontos, hogy a SARS-CoV-2-t neutralizáló GMT-k a 85. napig (63 nappal az emlékeztető után) stabilak maradtak, a titerek 120 és 181 között változtak, és így 1,3–1,9-szeres értéket értek el a neutralizáló konvaleszcens szérumpanel 94-es értékéhez képest.
Az S1-kötő IgG GMC-k az emlékeztető oltás után fokozatosan csökkentek, ami jellemző a proliferáció mintázatára, amelyet a természetes fertőzés vagy oltás által hasonló módon aktivált B-sejtek visszahúzódása követ25. Ezzel szemben a GMT-k szintje az emlékeztető oltás után kezdetben csökkent, de a 43. nap körül stabilizálódott, ami a funkcionális antitestek szelekcióját és affinitásérését jelenti.
A neutralizáló antitestek GMT-i szorosan korreláltak az S1-kötő IgG GMC-kkel (1.c ábra). Összefoglalva, a BNT162b2 által kiváltott neutralizációs válaszok és antigénkötő IgG-válaszok ebben a tanulmányban nagyrészt tükrözik az Egyesült Államok tanulmányában megfigyelteket, és először folytattak kiterjedt nyomon követést a 85. napig.
A nyilvánosan hozzáférhető információk alapján24 azonosított 18 SARS-CoV-2 RBD-variánsból álló panelt és a domináns nem RBD S D614G25 variánst értékelték a pszeudovírus neutralizációs vizsgálatokban meghatározott célpontokként. A szérumot hét nappal azután gyűjtötték, hogy a BNT162b2 emlékeztető dózisa magas neutralizációs titereket mutatott az egyes SARS-CoV-2 S-variánsok esetében (1.d ábra), ezzel igazolva a keringő vírustörzsek elleni neutralizáló válasz mértékét.
A vakcinával kiváltott T-sejt-válaszok prevalenciája és mértéke
37 olyan BNT162b2-vel immunizált résztvevő T-sejt-válaszát vizsgáltuk, akiktől elegendő perifériás vér mononukleáris sejt (PBMC) állt rendelkezésre: az oltás előtt (1. nap) és az emlékeztető oltást követően hét nappal (29. nap) elemeztük közvetlenül ex vivo IFN enzimhez kapcsolt immunoszorbens spot (ELISpot) eljárással (2. ábra, 5. kibővített adatábra, 2. kibővített adattáblázat).
A SARS-CoV-2 S egy szignálpeptidből (aa 1–13), az N-terminális S1 proteázfragmensből (aa 14–685) és a C-terminális S2 proteázfragmensből áll (aa 686–1273). Az S1 tartalmazza az RBD-t (aa 319–541), amely kötődik a gazdareceptorhoz, az S2 pedig a fúziót közvetíti a vírusburok és a sejtmembrán között. Az S-reaktivitás elkülönítéséhez az effektor CD4+ vagy CD8+ T-sejteket egy éjszakán át stimuláltuk egymással átfedő peptidekkel, amelyek a SARS-CoV-2 S vad típusú szekvenciájának különböző részeit reprezentálták, nevezetesen az N-terminális „1-es S-poolt” (aa 1–643) és „RBD”-t (aa 116 és az S aa 327–528 szakaszának fúziójával), valamint a C-terminális „2-es S poolt” (aa 633–1273).
2. ábra | A BNT162b2 indukálta T-sejt-válaszok előfordulása és nagysága
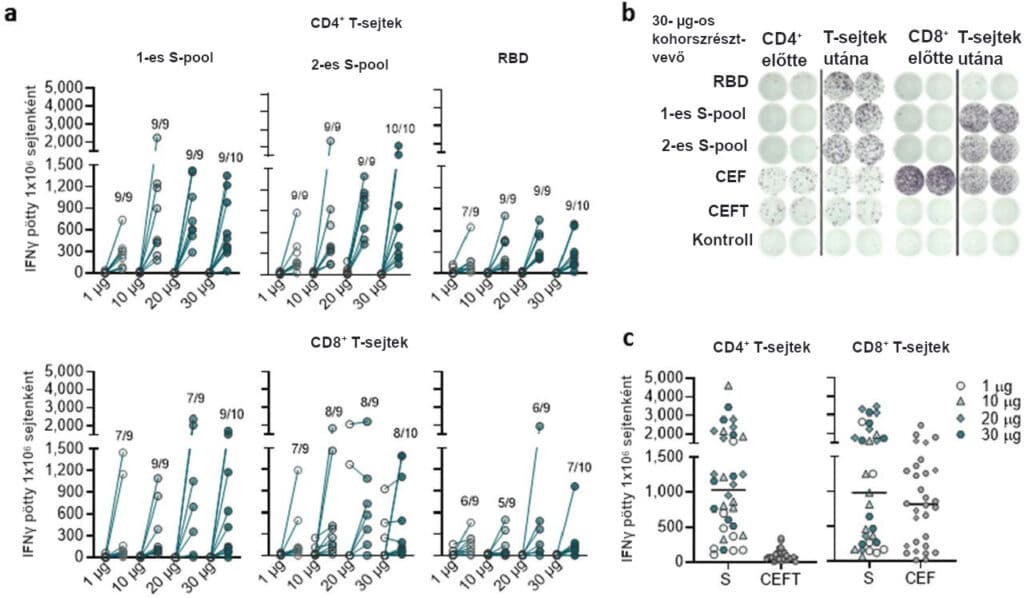
Az 1. napon (oltás előtt) és a 29. napon (7 nappal az emlékeztető után) nyert PBMC-ket (1, 10, és 20 µg dózis kohorsz esetén n=9; 30 µg-os dózis kohorsz esetén, n=10) CD4+ vagy CD8+ effektor T-sejtekkel dúsítottuk, és egész éjszakán át külön-külön stimuláltuk három, egymást átfedő peptidkészlettel, amelyek a SARS-CoV-2 S vad típusú szekvenciájának különböző részeit reprezentálták (N-terminális 1-es S-pool és RBD, valamint a C-terminális 2-es S-pool), közvetlen ex vivo IFNγ ELISpottal történő értékelés céljából. Gyakori kórokozó T-sejt-epitóp-poolokat, mint a CEF (immundomináns HLA I. osztályú CMV-epitópok, EBV, influenzavírus) és CEFT (immundomináns HLA II. osztályú epitópok CMV, EBV, influenzavírus, tetanusztoxoid), használtunk kontrollként. A sejttenyészet tápközege szolgált negatív kontrollként. Mindegyik pont két lyuk normalizált átlagát mutatja egyetlen résztvevőre, a csak tápközeges kontroll levonása után (a, c). a, Antigénspecifikus CD4+ és CD8+ T-sejt-válaszok az egyes dózis kohorszokhoz. Megadjuk azon résztvevők számát, akiknek a 29. napon kimutatható T-sejt-válaszuk volt, a dózis kohorszonkénti összes tesztelt résztvevő számával együtt. A 20 µg-os dóziskohorsz két résztvevőjének adatait nem sikerült normalizálni, és nem ábrázoljuk őket. b, példa a 30 µg-os dózis kohorsz résztvevőinek CD4+ és CD8+ ELISpot-jára. c, S-specifikus T-sejt-válaszok minden olyan résztvevőnél, akinek a mintája felismerte az S-peptidkészletet, valamint a kiindulási CEFT- és CEF-specifikus T-sejt-válaszok. A vízszintes sávok a medián értékeket jelzik.
Hét nappal a BNT162b2 bármely dózisban történő emlékeztetője után a SARS-CoV2 S-specifikus CD4+ T-sejtek nagy mennyiségben voltak kimutathatók mind a 37 résztvevőnél (2.a ábra, 5.a kibővített adatábra). Ezen résztvevők közül 34 esetében volt lehetséges az oltás előtti PBMC-k összehasonlítása. 34 alany közül harmincnak (88,2%) alakult ki de novo (a kiindulási állapotban nem létező) CD4+ T-sejt-válasza mind a SARS-CoV-2 1-es S-pool, mind 2-es S-pool ellen. Az egyik résztvevőnek csak a 2-es S pool ellen alakult ki de novo válasza. A fennmaradó három résztvevőnek de novo válasza alakult ki az 1-es S-pool ellen, és a már meglévő 2-es S-poollal szemben alacsony számú reaktív CD4+ T-sejtet lehetett kimutatni. Ebből a három résztvevőből kettőben a 2-es S-pool ellen már meglévő válaszokat oltással erősítették (91 és 188 pötty/106 oltás előtti sejt az oltás utáni 1391 és 965 pöttyhöz képest), míg a három résztvevő egyikében, a 2-es S-pool elleni előzetes válaszok stabilak maradtak (53–140 pötty/106 sejt). Összefoglalva, ezek az adatok azt mutatják, hogy a résztvevők 94,1%-ában (32/34) a BNT162b2 két dózisa poliepitópos CD4+ T-sejt-válaszokat (de novo vagy amplifikált) indukál mind az S N-, mind a C-terminális régiói ellen, és így az RBD-n kívüli epitópokkal szemben is (5.b kibővített adatábra).
Bár a ≥10 µg-os dózisszinteknél a CD4+ T-sejt-válasz nagysága nem tűnt dózisfüggőnek, egyénenként változó volt. A legerősebb válaszadókban az S-specifikus CD4+ T-sejt-válaszok meghaladták a közönséges vírusokra és a visszatérő antigénekre (citomegalovírus, Epstein-Barr-vírus, influenzavírus és tetanusztoxoid) adott memóriaválaszok több mint 10-szeresét (2.b, c ábra).
Vakcinával indukált S-specifikus CD8+ T-sejt-válaszokat 37 beoltott résztvevő közül 34-ben mutattak ki (91,9%). A többség erős válaszokat mutatott (2.a ábra, 5.a kibővített adatábra), amelyek összehasonlíthatók a citomegalovírus (CMV), az Epstein-Barr-vírus (EBV) és az influenzavírus (2.b, c ábra) elleni egyéni memóriaválaszokkal. A de novo S-specifikus CD8+ T-sejt-válaszok 33 résztvevőnél jelentek meg, amelyek vagy mindkettő (22 résztvevő), vagy az egyik S-pool ellen irányultak (tíz résztvevőből az 1-es S-poolra és két résztvevőből a 2-es S-poolra), ami a poliepitópos válasz túlsúlyát jelzi, beleértve a nem RBD S-specifikus T-sejteket (kiterjesztett adatok, 5.b ábra). Hét résztvevőnél a 2-es S-poolra már létező CD8+ T-sejt-válaszokat detektáltak, amelyeket az oltás nem fokozott tovább. A hét résztvevő közül hatnak volt egyidejű de novo válasza az 1-es S-poolra, amely erősségében nem különbözött szignifikánsan azokétól az egyénekétől, akik előzőleg nem reagáltak a 2-es S-poolra (5.c kibővített adatábra). Megjegyzendő, hogy a 34 kimutatható CD8+ T-sejt-válaszokkal rendelkező résztvevő közül a legerősebb válaszokat (magasabb, mint a harmadik kvartilis) az 1-es S-pool ellen figyeltük meg azoknál, akiknél korábban nem létezett a 2-es S-poolra specifikus válasz.
Az S-specifikus CD4+ T-sejt-válaszok nagysága pozitívan korrelált az S1-kötő IgG-vel (kiterjesztett adatok, 6.a ábra), és az intramolekuláris segítség fogalmával 26 összhangban az S-specifikus CD8+ T-sejt-válaszok erősségével is (6.b kibővített adatábra). Az S-specifikus CD8+ T-sejt-válaszok szintén pozitívan korreláltak az S1-kötő IgG-vel (6.c kibővített adatábra), jelezve a humorális és a celluláris adaptív immunitás konvergens fejlődését.
A vakcina kiváltotta T-sejt-válaszok polarizációja
Az S-specifikus T-sejtek funkcionalitásának és polarizációjának értékeléséhez az 1-es S-pool, a 2-es S-pool és az RBD-pool stimulációjára válaszként termelődő citokineket IFNγ-, IL-2- és IL-4-re specifikus intracelluláris festéssel (ICS) határoztuk meg a 37 BNT162b2-vel immunizált résztvevő oltás előtti és utáni PBMC-iben (2. kibővített adattáblázat). A vakcina által kiváltott S-specifikus CD4+ T-sejtek jelentős része szekretálta az IFNy-t, az IL-2-t vagy mindkettőt, míg a Th2-citokin IL-4-et szekretáló T-sejtek alig voltak kimutathatók (3.a–c ábra, 5.d,e kibővített adatábra). A vakcinával indukált S-specifikus CD8+ T-sejtek túlnyomórészt IFNy-t és alacsonyabb mértékben IL-2 szekretáltak az 1-es S-pool és a 2-es S-pool stimulációjára válaszul. Az 1-es S-poolra specifikus IFNy+ CD8+ T-sejtek frakciói az összes perifériás vér CD8+ T-sejtjének körülbelül 1%-át tették ki (3.d ábra). Megjegyzendő, hogy az elemzett résztvevők közül többen (n=3 a 20 µg-os és n=3 a 30 µg-os dóziskohorszban) korábban már létező 2-es S-poolra specifikus CD8+ T-sejt-válaszokat mutattak, amelyek a 6 résztvevő közül 5-ben nem erősödtek tovább az oltás után. Erős, már meglévő 2-es S-poolra specifikus IFNy+ CD4+ T-sejt-válasz volt kimutatható egy résztvevőnél (20 µg dóziskohorsz) (3.c ábra).
3. ábra | A BNT162b2 indukálta T-sejtek citokinpolarizációja
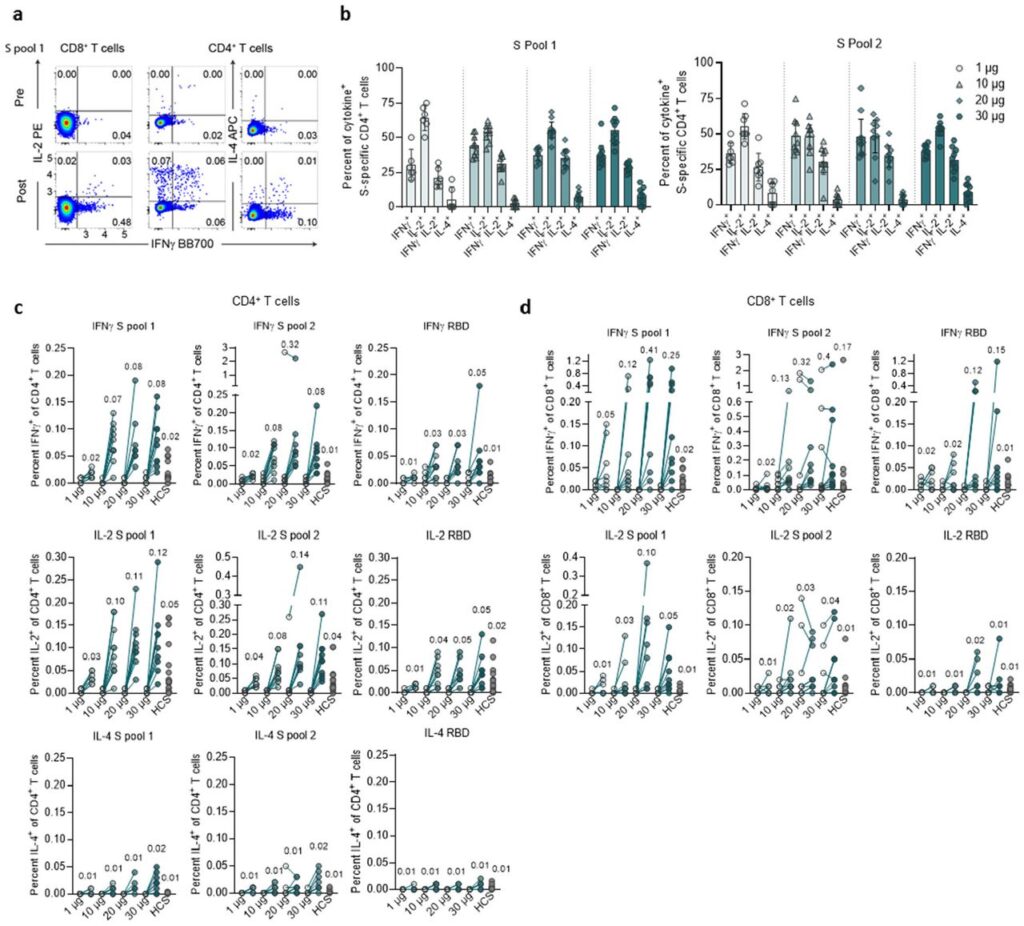
Az 1. napon (az első oltás előtt) és a 29. napon (az emlékeztetőt követő 7. napon) kapott PBMC-ket (dózis kohorszok 1 µg, n=8; 10 és 30 µg, mindkettőnél n=10; 20 µg, n=9) és COVID19-ből felépültek donorsejtjeit (HCS, n=18; c, d) egy éjszakán át stimuláltuk három, egymást átfedő peptidkészlettel, amelyek a SARS-CoV-2 S vad típusú szekvenciájának különböző részeit reprezentálták (N-terminális poolok: 1-es S-pool [aa 1–643] és RBD [aa 1–16 fuzionálva az aa 327–528 szakaszával], és a C-terminális 2-es S-pool [aa 633–1273]), és áramlási citometriával elemeztük (a kapuzási stratégiát lásd az 1. kiegészítő ábrán). a, Példa a 30 µg-os dóziskohorsz résztvevőjének citokintermelő CD4+ és CD8+ T-sejtjeinek az 1-es S-pool-ra adott válaszának színezett áramlási citometriás felhődiagramjára. b, Az S-specifikus CD4+ T-sejtek, amelyek a jelzett citokint termelik az összes citokintermelő S-specifikus CD4+ T-sejt frakciójaként, válaszul az 1-es S-pool-ra és a 2-es S-pool-ra. A CD4-re nem reagálók (<0,03%-a összes citokintermelő T-sejtnek: 1 µg, n=2 [1-es S-pool] és n=1 [2-es S-pool]; 10 µg, n=1) kizárásra kerültek. Számtani átlag 95%-os konfidenciaintervallummal. c, S-specifikus CD4+ (1-es S-pool, 2-es S-pool és RBD) és d, CD8+ T-sejtek (1-es S-pool, 2-es S-pool és RBD), amelyek a jelzett citokint termelik, az ugyanazon részhalmaz összes keringő T-sejtjeinek frakciójaként ábrázolva. Az adatpontok feletti értékek a dózis kohorszonkénti átlagos frakciókat jelzik. A résztvevők PBMC-it egyben teszteltük (b-d).
Mindkét vizsgálati rendszerben a CD4+, valamint a CD8+ T-sejtek citokintermelése a teljes SARS-CoV-2 S-t tartalmazó peptidkészletekre adott válaszként meghaladta az RBD-peptidkészlet elleni válaszokat, ami még inkább igazolta a kiváltott T-sejt-válaszok poliepitópos jellegét, amit a BNT162b2 indukált. A BNT162b2 kiváltotta S-specifikus IFN+ vagy IL-2+ CD4+ és CD8+ T-sejtek átlagfrakciója az összes keringő T-sejthez képest magasabb volt, mint a tizennyolc kontrollalanynál, akik felépültek a COVID19-ből (HCS) (3.c, d ábra).
A CD8+ T-sejtek epitópspecifitása és fenotípusa
A CD8+ T-sejt-válaszokat epitópszinten jellemeztük három BNT162b2-vel oltott résztvevőnél. Ebből a célból az oltás előtti és utáni PBMC-ket egyéni peptid/MHC-multimer-festő keverékekkel festettük az áramlási citometriás elemzéshez. 23 (4 HLA-B*0702, 19 HLA-A*2402), 14 (HLA-B*3501) és 23 (7 HLA-B*4401, 16 HLA-A*0201) különféle peptid/MHC-allélpárt használtunk az 1., a 2. és a 3. résztvevő esetében. Ez a megközelítés azonosította a de novo indukált CD8+ T-sejtek reaktivitását több epitóp ellen minden egyes résztvevő esetében, összeadva összesen nyolc különböző epitóp/MHC-pár eloszlását az S teljes hosszúságán (4.a, c ábra). Az epitóp-specifikus T-sejtek-válaszainak nagysága a perifériás CD8+ T-sejtek esetében 0,01-3,09% között mozgott, és a legnagyobb kiterjedést a HLA-A*0201 YLQPRTFLL (CD8+ multimer+ 3,09%-a), HLA-A*2402 QYIKWPWYI (CD8+ multimer+ 1,27%-a) és HLA-B*3501 QPTESIVRF (CD8+ multimer+ 0,17%-a) esetében figyelték meg.
4. ábra | A BNT162b2 indukálta T-sejtek jellemzése egyetlen epitóp szinten
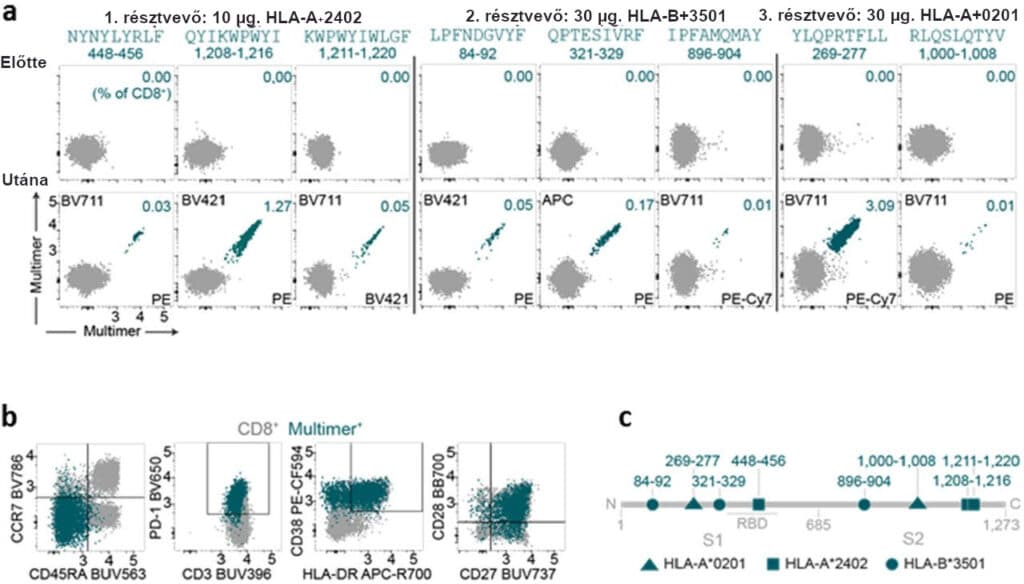
Három oltott résztvevő 1. napon (az első oltás előtti) és 29. napon (7 nappal az emlékeztető után) nyert PBMC-it (dózis kohorszok 10 µg, n=1; 30 µg, n=2) egyedi pMHC I. osztályú multimer-keverékekkel festettük és áramlási citometriával elemeztük a T-sejt epitóp-specifitását (a) és fenotípusát (b; példa a 3. résztvevőtől; YLQPRTFLL) (a kapuzási stratégiát lásd a 2. kiegészítő ábrán). A felhődiagramok feletti peptidszekvenciák a pMHC I. osztályú multimer epitóp-specificitást, a felhődiagramok fölötti számok az S-epitópján található aminosavakat jelzik. c, Az azonosított MHC I. osztályra korlátozott epitópok lokalizációja az S-en belül.
Mivel a pMHC-multimer megközelítés a potenciális válaszok elkülöníthető részcsoportjait vizsgálja, az ELISpot és az ICS által meghatározott teljes S-re adott tömeges IFNγ+ CD8+ T-sejt-válaszok átfogóan vizsgálják a poliepitópos T-sejt-választ. Azonban mindkét adatsor összehasonlítása azt mutatta, hogy egy funkcionális T-sejt-vizsgálat alul becsülheti a sejtes immunválasz valódi mértékét (5.f kibővített adatábra).
A pMHC multimer+ S-antigénnel találkozott CD8+ T-sejtek specificitásának fenotipizálása korai, differenciált effektormemória-fenotípust fedett fel, amelyre a CCR7 és CD45RA alacsony expressziója, valamint a CD28 és CD27 kostimulációs molekulák magas expressziója volt jellemző A CD8+ T-sejtek expresszálták a rokonaktivációval összefüggő markereket is, mint például a CD38, a HLADR és a PD-1 (4.b ábra).
Megbeszélés
Az adaptív immunrendszer effektorainak kiegészítő szerepe van a vírusfertőzések elleni védelemben. Míg a neutralizáló antitestek jelentik az első védelmi vonalat, a CD8+ citotoxikus T-limfociták (CTL-ek) hozzájárulnak a vírusclearance-hez az intracelluláris kompartmentekből, amelyek elérhetetlenek a neutralizáló antitestek számára. Az antigénspecifikus CD4+ T-sejtek immunszervező funkcióval rendelkeznek, ideértve a közösen tevékenykedő B-sejtek és a CD8+ T-sejtek működését, a memóriaképzés támogatását, valamint a közvetett (pl. IFNy-n keresztüli) vagy közvetlen (MHC II. osztályt expresszáló célsejtek elleni) citotoxikus aktivitást.
A folyamatban lévő klinikai vizsgálatok előkészítésében széles körű egyetértés van abban, hogy egy COVID19-oltóanyagnak antitesteket kell indukálnia a SARS-CoV-2 S ellen. Azt azonban még nem tudjuk, hogy az antitestválaszok elegendőek lesznek-e a SARS-CoV-2 elleni teljes és tartós védőimmunitáshoz, és a SARS-CoV-2-specifikus T-sejtek mennyiben járulnak hozzá ehhez.
Az ehhez szorosan kapcsolódó első SARS-CoV-val kapcsolatos tapasztalatok azt sugallják, hogy a T-sejtek megakadályozzák a betegség súlyos formáit,27 és a hosszú távú védelemmel lehetnek összefüggésben28,29. Az újfajta SARS‐CoV‐2 esetében a fertőzött és konvaleszcens egyének immunitási mechanizmusainak megértése csak most kezd körvonalazódni. Egyre több adat támasztja alá a T-sejtes immunválasz szerepét30-32. A kritikus állapotú COVID19-betegek esetében beszámoltak arról, hogy hiányoznak az S1-reaktív CD4+ T-sejtjeik33. A tünetmentes vírusexpozíció esetei összefüggést mutatnak a szerokonverzió nélküli celluláris immunválaszokkal, ami azt jelzi, hogy a SARS-CoV-2-specifikus T-sejtek neutralizáló antitestek hiányában is relevánsak lehetnek a betegség elleni védekezésben29.
Ebben a jelentésben beszámolunk arról, hogy a BNT162b2-vel történő oltás összehangolt immunválaszt vált ki a SARS-CoV-2 S-specifikus neutralizáló antitestekkel, a CD4+ és a CD8+ T-sejtekkel, valamint az immunmoduláló citokinekkel, mint az IFNy.
Valamennyi BNT162b2-vel oltott résztvevő de novo S-specifikus CD4+ T-sejt-válaszokat adott, és a résztvevők majdnem 92%-ánál jelentek meg a CD8+ T-sejt-válaszok, amelyeket ex vivo ELISpot eljárással detektáltak. A T-sejt-válaszok nagysága egyénenként változott, és nem mutatott egyértelmű dózisfüggést. Még a legalacsonyabb 1 µg-os BNT162b2 dózis mellett is a beoltott résztvevők többségénél a CD4+ és CD8+ T-sejtek erőteljes expanziója volt megfigyelhető. A T-sejt-válaszokat az RBD, az S1 és az S2 S-régiók ellen irányítottuk, jelezve a több független MHC-I és -II-epitóp immunfelismerését, amely az egyik oka volt annak, hogy a BNT162b2-t előnyben részesítsük a BNT162b1-gyel szemben.
Az IFNy és az IL-2 expressziója, illetve az IL-4 alacsony szintje a BNT162b2 által indukált CD4+ T-sejtekben a Th1-profilt és a potenciálisan káros Th2-immunválasz hiányát jelzi.
Míg az S S1-alegységével szembeni összes CD8+ T-sejt-válaszok de novo alakult ki, és a kiindulási állapotban nem volt kimutatható, az S2-alegységgel szemben már meglévő immunválaszokat több egyénnél azonosítottunk. Az S1-fragmens kisebb szekvenciahomológiát mutat a megfelelő szezonális koronavírus-szekvenciákkal, mint az S2-fragmens, ami azt jelzi, hogy esetlegesen előzetesen már jelenlevő keresztreaktív CD8+ T-sejteket észlelhettünk34,35.
A pMHC-multimer-technológia lehetővé tette az oltással indukált CD8+ T-sejtek által felismert S-epitópok azonosítását éppúgy, mint az adott epitópspecifikus T-sejtek közvetlen mennyiségi meghatározását. Az egyes résztvevők kumulatív T-sejt-gyakoriságai meghaladták az ELISpot és ICS vizsgálatokban mért teljes T-sejt-választ, jelezve, hogy azok a vizsgálatok alábecsülik a poliepitópos válasz valódi nagyságát. Az egypeptid-analízisről jól ismert, hogy magasabb T-sejt-gyakoriságokat eredményez, összehasonlítva a funkcionális T-sejt-vizsgálatokkal, amelyek peptidkészletekkel stimulálnak, immunogén epitópok sokaságával versengve. Az indukált CD8+ T-sejtek nagy hányada korai differenciált effektor-memóriasejt volt. Ez a kedvező fenotípus képes gyorsan reagálni, de korlátozott kapacitással rendelkezik az IFNy termelésére, így kevésbé valószínű, hogy a funkcionális T-sejt-vizsgálatokban kimutatható lenne. Korábbi tanulmányok azonosítottak olyan epitópokat a SARS-CoV-2 S-en, amelyekkel szemben a fertőzött egyénekben a CD8+ T-sejtek száma megnőtt36,37. Tudomásunk szerint ez az első jelentés az epitópokról, amelyeket a COVID19-vakcinával indukált T-sejtek felismernek. Megjegyzendő, hogy a vizsgálatunk során azonosított, immunológiai szempontból domináns HLA-A*02:01 restrikciós YLQPRTFLL peptidet korábban már leírták konvaleszcens COVID19-betegeknél36,37.
Amellett, hogy új betekintést nyújt a T-sejt-válaszokba, ez a tanulmány megismétli a korábbi, az USA-ban végzett vizsgálatainkban tett megállapításokat1, és megerősíti az előnyös biztonsági profilt, valamint azt, hogy az antitestválaszok nagymértékben kiváltódnak, ez utóbbit hosszabb ideig, a 85. napig követtük nyomon (63 nappal az emlékeztető oltás után). A 10-30 µg BNT162b2-vel végzett első/emlékeztető oltás olyan GMT-ket váltott ki, amelyek a kezdeti csökkenés után a 85. napig stabilak vagy magasabbak maradtak, mint a COVID19-ből felépült egyének GMT-i. A BNT162b2 immunszérumok 19 pszeudotipizált vírust neutralizáltak hatékonyan (ezek közül 18 különböző RBD-variánsú S-fehérjét használva lép be a sejtekbe, és egyikük a D614G domináns S-variánst használja), ami jelzi, hogy a BNT162b2 által kiváltott védelem széleskörű lehet a jelentett mutációkkal szemben1,9,10.
Klinikai vizsgálatunk korlátai közé tartozik a kis mintanagyság, a fontos populációk (pl. idősebb felnőttek, más etnikumok, immunhiányos egyének és gyermekpopulációk) reprezentációjának hiánya, valamint a vérminták korlátozott rendelkezésre állása a mélyebb T-sejt-elemzéshez.
Az antigénnel aktivált B- és T-sejtek általában proliferáción mennek keresztül, majd visszahúzódó kontrakció következik be, mialatt a számuk fokozatosan csökken, mielőtt a hosszútávú memóriafázisba lépnének22,23, azonban az ebben a cikkben bemutatott rövidtávú nyomon követés nem teszi lehetővé az immunválaszok extrapolálását a hosszútávú tartósságra. Bár biztató, hogy a BNT162b2 robusztusan aktiválja az antigénspecifikus humorális és celluláris immuneffektor-rendszereket, nem világos, hogy ez az immunválasz-mintázat megvéd-e a SARS-CoV-2-fertőzéstől és megakadályozza-e a COVID19-et. Ezekkel a kérdésekkel foglalkozik a folyamatban lévő klinikai vizsgálat, amely magában foglalja a két folyamatban lévő I./II. fázisú vizsgálat résztvevőinek hosszabb távú nyomon követését, egy dedikált immunbiomarker-vizsgálatot az immunválasz összetett elemeinek további részletes vizsgálatára, valamint a folyamatban lévő II./III. fázisú vizsgálatot a hatásossági végpontokkal.
Köszönetnyilvánítás
Köszönjük Mikael Dolsten, a Pfizer tudományos vezérigazgatójának tanácsát a kézirat elkészítése során. Köszönetet mondunk C. Andersnek, C. Anft, N. Beckmannak, K. Bissingernek, P. Cienskowskinak, K. Clarke-nak, C. Eckernek, A. Engelmannak, M. Fiereknek, D. Harjantonak, A. Heinennek, M. Hossainzadeh-nek, S. Jägle-nek, L. Jecknek, O. Kahlnak, D. Kallinnak, M. Knezovicnak, T. Koturnak, M. Kretschmernek, A. Kruithofnak, J. Mc Gee-nek, B. Mehlhase-nek, C. Müllernek, S. Murphy-nek, L.-M. Schmidnek, K. Schmoldtnak, R. Schulz-nak, L. Srinivasannak, M. Vereschildnek, T. Weisenburgernek és S. Wesselnek a technikai támogatásért, a projektmenedzsmentért és a tanácsadásért. Köszönjük P. Kochnak az adatkezelést és elemzést. Köszönjük O. Kistner, S. Liebscher, J. Loschko és K. Swanson szakértői tanácsát. Köszönjük Judith Absalonnak a kézirattal kapcsolatos tanácsokat. Köszönetet mondunk a CRS csapatának (Mannheim és Berlin) a tanulmány elvégzéséért: S. Armaninak, M. Berse-nek, M. Casjens-nek, B. Ehrlichnek, F. Seitz-nek, M. Streckebeinnek. Köszönetet mondunk W. Kalinának, I. Scully-nak, a Pfizer Vaccines Clinical Assays Teamnek és a Pfizer Aviation Teamnek a szerológiai elemzések technikai és logisztikai támogatásáért. Köszönjük a GISAID Nucleotide adatbázisnak a SARS-CoV-2 teljes genomszekvenciáinak megosztását.
Szerzői hozzájárulások
U.S. gondolta át és fogalmazta meg a stratégiát Ö.T. támogatásával. A kísérleteket N.B., E.D., C. F.-G, C.A.K., U.L., A.M., J.Q., P.-Y.S., A.U. tervezték vagy felügyelték, és I.V. A.B., N.B., D.C., M.C., C. F.-G, K.P., J.Q., A.U. és P.-Y.S. hajtotta végre a kísérleteket. D.B., S. Brachtendorf, E.D., P.R.D., J.G., K.U.J., A.-K.E., P.K., M.T., L.M.K., M.-C.K., V.L., A.M., J.Q., J.S., N.B., A.U., I.V. és M.V. az adatokat elemezte. A.P. prioritásként kezelte az epitópokat a multimervizsgálathoz. J.Z.D. felügyelt a multimer-vizsgálathoz előállított peptidek gyártására és szállítására. D.M. tervezte és felügyelte a táblázatokat a klinikai vizsgálatok adatainak elemzéséhez. R.H. felelős az adatok normalizálásáért és adaptálásáért. C.B, L.H. és C.R. voltak felelősek a biomarkerekért és a K+F-programok irányításáért. G.B., K.K., A.J.M., J.R. és G.T.S. optimalizálta az mRNS tulajdonságait. A.K-B., S. Baumann, A.S., D.L., M.B., S. Bolte és T.P. a klinikai vizsgálat összehangolt operatív lebonyolítását végezte. J.L.P. tanácsot adott a vizsgálathoz. U.S. és Ö.T., akiket M.B., N.B., E.D., P.R.D., K.U.J., L.M.K., A.M., A.U., I.V. és M. V. támogatott, értelmezte az adatokat és írta meg a kéziratot. Minden szerző részt vett a kézirat áttekintésében.
Összeférhetetlenségi nyilatkozat
A szerzők kijelentik: U.S. és Ö.T. a BioNTech SE (Mainz, Németország) igazgatósági tagjai és alkalmazottai; A. K.-B., A.-K.E., A.U., C.R., D.B., P.K., D.L., D.M., E.D., J.G., J. S., M.-C.K., R.H., S. Bolte, S. Brachtendorf, T.P., U.L. és V.L. a BioNTech SE alkalmazottai; A.J.M., A.M., G.B., G.T.S., I.V., J.R., J.Q., K.K., L.M.K., N.B. és M.V. a BioNTech RNA Pharmaceuticals GmbH alkalmazottai; A.P. és J.Z.D a BioNTech US alkalmazottai; M.B. a Bexon Clinical Consulting LLC alkalmazottja. A.B., C.A.K. és K.P. a Regeneron Pharmaceuticals Inc. alkalmazottai; A.M., K.K., Ö.T. és U.S. az RNS technológiával és a COVID19 vakcinával kapcsolatos szabadalmak feltalálói és alkalmazói; A.K.-B., J.Z.D., A.J.M., A.M., C.R., G.B., D.B., D.L., E.D., I.V., J.G., K.K., L.M.K., A.P., M.V., N.B., Ö.T., R.H., S. Bolte, U.L. és a U.S: a BioNTech SE részvényesei; D.C., M.C., P.R.D., K.U.J. és J.L.P. a Pfizer alkalmazottai és rendelkezhetnek a Pfizer értékpapírjaival; C.A.K. a Regeneron Pharmaceuticals, Inc. hivatalnoka; A.B., C.A.K. és K.P. rendelkeznek a Regeneron Pharmaceuticals, Inc. értékpapírjaival; C.F.-G. és P.-Y.S. kompenzációt kapott a Pfizertől a neutralizációs vizsgálat elvégzéséért; ezen kívül nincsen semmilyen más kapcsolat vagy tevékenység, amely befolyásolhatná a beküldött munkát.
Pénzügyi támogatás
A BioNTech a vizsgálat szponzora, és felelős a vizsgálati elrendezésért, az adatgyűjtésért, az adatelemzésért, az adatértelmezésért és a jelentés megírásáért. A Pfizer tanácsadóként vett részt a vizsgálatban és a kézirat elkészítésében, szerológiai adatokat állított elő és szerződött a szerológiai adatok előállítására. A levelező szerzők teljes hozzáféréssel rendelkeztek a vizsgálat összes adatához, és végső felelősséggel tartoztak az adatok közzététel céljából történő benyújtásáért. Minden vizsgálati adat minden szerző részére rendelkezésére állt.
Ez a tanulmány a benyújtáskor semmilyen külső finanszírozásban nem részesült.
További információk
Kiegészítő információk állnak rendelkezésre ehhez a cikkhez.
A levelezést és az anyagokkal kapcsolatos kéréseket Ugur Sahinnak kell címezni.
Anyagok és módszerek
Klinikai vizsgálati elrendezés.
A BNT162-01 (NCT04380701) vizsgálat egy folyamatos, ernyőtípusú (umbrella), emberen először végzett, I/II. fázisú, nyílt elrendezésű, dózistartományos klinikai vizsgálat, amelyben a különböző intramuszkulárisan növekvő dózisszintek biztonságosságának, tolerálhatóságának és immunogenitásának értékelésére beadott BNT162 mRNS vakcinajelölteket vizsgáltak egészséges férfiak és nem terhes nők körében, 18-55 éves korig (módosítva az 56-85 éves korosztály hozzáadásával). A vizsgálat fő végpontjai a biztonságosság és az immunogenitás. A legfontosabb kizárási kritériumok közé tartozott a COVID19 korábbi klinikai vagy mikrobiológiai diagnózisa; felírt gyógyszerek a COVID19 megelőzésére; korábbi oltás bármely koronavírus-vakcinával; pozitív szerológiai teszt a SARS-CoV-2 IgM-re és/vagy IgG-re; és a SARS-CoV-2 nukleinsav-amplifikációs teszt (NAAT)-pozitivitás orrból vett mintából; a fokozott súlyos COVID19-kockázat; és az immunhiányos egyének.
A bemutatott adatok a BNT162b2-vel immunizált egészséges felnőttekből származnak, akik 19-55 évesek voltak, 1, 10, 20 vagy 30 μg dózisszintnek kitéve. Az adatok előzetes elemzésen alapulnak (az adatkinyerés dátuma 2020. október 23. a biztonságossági és antitest-elemzéshez, 2020. október 16. és 2020. november 24. a T-sejt-elemzéshez [intracelluláris citokinfestés és ELISpot]), és a vakcina által kiváltott immunogenitás elemzésére összpontosítanak, amelyeket leíró jelleggel a különböző időpontokban, valamint a reaktogenitással kapcsolatban foglaltunk össze. Az összes résztvevőt, akivel kapcsolatban rendelkezésre álltak adatok, bevontuk az immunogenitási elemzésekbe. A vizsgálat ezen részét egy németországi helyszínen végeztük, dózisszintenként 12 egészséges résztvevővel, dózisnövelés/-csökkentés elrendezéssel.
A sentineladagolást minden dózisemelési kohorszban elvégeztük. Ebben a kohorszban való előrehaladás és a dózisnövelés megkövetelte az adatok felülvizsgálatát a biztonságossági felülvizsgálati testület részéről. A résztvevők a BNT162b2 első dózisát az 1. napon kapták, az emlékeztetőt a 22±2. napon (egyetlen résztvevő a 28. napon a 10 µg-os dóziskohorszból). Az antitestvizsgálatokhoz a szérumot az 1. (első oltás előtt), a 8±1. (első oltás után), 22±2. (emlékeztető előtt), 29±3., 43±4. és 50±4. napon (emlékeztető után) vettük. A T-sejt-vizsgálatokhoz a PBMC-ket az 1. (első oltás előtt) és a 29±3. napon (emlékeztető után) vettük (1. kibővített adatábra). A résztvevők nyomon követése folyamatban van, és magába foglalja az antitest- és a T-sejt-válaszok értékelését későbbi időpontokban. A reaktogenitást betegnapló segítségével értékeltük. Két résztvevőt kizártunk a vizsgálatból az emlékeztető oltás előtt, egy ezzel a vizsgálati készítménnyel nem összefüggő ok (az 1 µg-os dóziskohorsz résztvevője) és egy nemkívánatos esemény (a 10 µg-os dóziskohorsz résztvevője) (felső légúti tünet) miatt. A vizsgálatot Németországban, a Helsinki Nyilatkozat és a Helyes Klinikai Gyakorlat iránymutatásainak megfelelően, valamint egy független etikai bizottság (Ethik-Kommission, Landesärztekammer, BadenWürttemberg, Stuttgart, Németország) és az illetékes szabályozó hatóság (Paul-Ehrlich Institute, Langen, Németország) jóváhagyásával hajtottuk végre. Minden résztvevő írásos beleegyezését adta a vizsgálathoz.
Az RNS előállítása.
A BNT162b2 egy Helyes Gyártási Gyakorlatnak megfelelő (GMP) mRNS-hatóanyagot tartalmaz, amely a trimerizált SARS-CoV-2 S-glikoprotein RBD-antigénjét kódolja. Az RNS-t DNS templátból állítjuk elő in vitro transzkripcióval, uridin-5’-trifoszfát (UTP) helyett 1-metil-pszeudouridin-5’-trifoszfát (m1ΨTP; Thermo Fisher Scientific) jelenlétében. A sapkázást (capping) ko-transzkripcióval hajtjuk végre egy trinukleotid-sapka-1-analóg ((m27,3’O)Gppp (m2’-O)ApG; TriLink) segítségével. Az antigént kódoló RNS olyan szekvenciaelemeket tartalmaz, amelyek növelik az RNS stabilitását és a transzlációs hatékonyságot az emberi dendritikus sejtekben11,12. Az mRNS-t lipidekkel formulázzuk az RNS-LNP vizsgálati készítmény előállításához. A vakcinát pufferolt folyadékoldatként szállítottuk az i.m. injekcióhoz, amit -80°C-on tároltunk.
Fehérjék és peptidek.
Két 15-mer peptidkészletet, átfedésben 11 aminosavval (aa) és együttesen lefedve a vad típusú SARS-CoV-2 S teljes szekvenciáját (1-es S-pool az aa 1–643-re, a 2-es S-pool az aa 633-1273-re), illetve egy olyan poolt, amely a SARS-CoV-2 RBD-t (aa 327–528) fedi le az S N-terminálisához fuzionált szignálpeptiddel (aa 1–16), PBMC-k ex vivo stimulációjára, használtunk az áramlási citometriához és az IFNy ELISpot-hoz. A CEF-et (CMV, EBV, influenzavírus; humán leukocita antigén [HLA] I. osztályú epitóp-peptidkészlet) és CEFT-t (CMV, EBV, influenzavírus, tetanusztoxoid; HLA II. osztályú epitóp-peptidkészlet) használtuk kontrollként az általános T-sejt-reaktivitás és a memória T-sejt-válaszok nagyságának meghatározásához. Az összes fenti peptidet a JPT Peptide Technologies cégtől szereztük be. Az easYmer vizsgálatokban használt 8–12 aminosav hosszú peptideket a BioNTech US gyártotta.
Humán konvaleszcens szérum és PBMC-panel.
SARS-CoV-2-fertőzött betegek szérumát/COVID19 konvaleszcens szérumot (n=38) gyűjtöttünk 18-83 éves donoroktól legalább 14 nappal a PCR-rel megerősített diagnózis után olyan időpontban, amikor a résztvevők tünetmentesek voltak. A donorok átlagéletkora 45 év volt. A neutralizáló GMT-k a donorok alcsoportjaiban a következők voltak: tünetes fertőzöttek, 90 (n=35); tünetmentes fertőzöttek, 156 (n=3); kórházba került betegek, 618 (n=1). A szérumokat a Sanguine Biosciencestől (Sherman Oaks, Kalifornia), az MT Grouptól (Van Nuys, Kalifornia) és a Pfizer Occupational Health and Wellnesstől (Pearl River, New York) szereztük be. SARS-CoV-2-fertőzött betegek szérumát/COVID19 konvaleszcens PBMC mintákat (n=18) gyűjtöttünk a 22-79 éves donoroktól 30-62 nappal a PCR-rel megerősített diagnózis után, amikor a donorok tünetmentesek voltak. A PBMC-donorok tünetmentesek voltak vagy enyhe fertőzésben szenvedtek (n=16, klinikai pontszám: 1 vagy 2), vagy kórházba kerültek (n=2, klinikai pontszám: 4 vagy 5). A vérmintákat a Frankfurt University Hospitaltól kaptuk.
Sejttenyésztés és primer sejtek izolálása.
A Vero-sejteket (American Type Culture Collection [ATCC] CCL-81) és a Vero-E6-sejteket (ATCC CRL-1586) Dulbecco módosított Eagle médiumban (DMEM) tenyésztettük GlutaMAX™-szal (Gibco) és 10% fötális borjúsavóval (FBS) (Sigma-Aldrich) kiegészítve. A sejtvonalakat megvizsgálták a mikoplazma-fertőzés szempontjából beérkezés után, valamint az tenyésztés és a fagyasztás előtt. A PBMC-ket Ficoll-Paque™ PLUS (Cytiva) sűrűséggrádiens-centrifugálással izoláltuk, és az analízisig lefagyasztottuk.
S1- és RBD-kötő IgG-eljárás.
A C-terminális Avitag™-ot (Acro Biosystems) tartalmazó rekombináns SARS-CoV-2 S1-et vagy RBD-t sztreptavidinnel bevont Luminex mikrogömbökhöz kötöttük. A résztvevők hővel inaktivált szérumait 1:500, 1:5000 és 1:50 000 arányban hígítottuk. Egy éjszakán át 2–8°C-on végzett rázatva inkubálás után a lemezeket 0,05%-os Tween-20-at tartalmazó oldatban mostuk. Kecske-antihumán másodlagosan jelölt fluoreszcens poliklonális antitest (Jackson Labs) hozzáadása után 90 percig szobahőmérsékleten rázattuk, majd a lemezeket még egyszer 0,05%-os Tween-20-at tartalmazó oldatban mostuk. Az adatokat medián fluoreszcenciaintenzitásként (MFI) rögzítettük a Bioplex200 rendszerrel (Bio-Rad), és referencia standardgörbe segítségével megállapítottuk az U/ml-be átszámított antitest-koncentrációkat, önkényesen meghatározott 100 U/ml koncentrációval és a szérumhígítási-tényezővel számolva. A referenciastandard öt konvaleszcens szérumminta készletéből állt, amelyet 14 nappal a COVID19 PCR-rel felállított diagnózisa után vettünk le, és szekvenciálisan hígítottuk antitesthiányos emberi szérumban. Három hígítást alkalmaztunk annak a valószínűségnek növelésére, hogy bármely minta legalább egyik eredménye a standardgörbe használható tartományába essen. A vizsgálati eredményeket U/ml IgG-ben adtuk meg. A végső vizsgálati eredményeket az összes mintahígítás geometriai átlagkoncentrációjaként fejeztük ki, amely érvényes vizsgálati eredményt adott a vizsgálati tartományon belül.
SARS-CoV-2 neutralizációs eljárás.
A neutralizációs eljárás során a SARS-CoV-2 egy korábban leírt törzsét használtuk (USA_WA1/2020), amelyet reverz genetikai módszerrel izoláltak és a genomját a hetedik nyitott leolvasási keretbe (ORF) beépített mNeonGreen (mNG) génnel módosították38. Ez a riporterkonstrukció a vad típusú vírustól nem megkülönböztethető plakkmorfológiát és növekedési görbét mutat. A virális törzsoldat (2×107 PFU/ml) Vero-E6-sejteken növesztve készült a korábbi leírásnak megfelelően38. A fluoreszcenciaalapú neutralizációs eljárás hasonló eredményt hozott, mint a hagyományos plakkredukciós neutralizációs eljárás39 a betegek konvaleszcens szérumának vizsgálatakor. A hőinaktivált szérumból készült hígítási sort a riportervírussal együtt 1 órán át, 37°C-on inkubáltuk (2×104 PFU lyukanként, ahhoz, hogy az egy sejtrétegű Vero CCL81-on a 10–30%-os infekciós rátát elérjük), mielőtt az egy sejtrétegű Vero CCL81 beoltottuk volna vele (amely tenyésztésekor arra törekedtünk, hogy 8000–15 000 sejt jusson a lemez minden lyukának központi területére a szélesztéskor, 24 órával a vírusfertőzést megelőzően). 96-lyukú lemezeket használtunk a fertőzött sejtek számának pontos kvantifikációja érdekében. Az egyes lyukakban a teljes sejtszámot sejtmagfestéssel (Hoechst 33342) határoztuk meg, a vírusok által megfertőzött gócokat 16–24 órával a beoltást követően Cytation 7 Cell Imaging Multi-Mode Reader készüléken (BioTek) a 3.09-es verziószámú Gen5 Image Prime szoftver segítségével vizsgáltuk. A titereket a 8.4.2-es verziószámú GraphPad Prism szoftverrel számoltuk a szérum egyes koncentrációin mérhető neutralizációs képesség százalékos értékére illesztett négyparaméteres logisztikus (4PL) illesztésű modellekkel. Az 50%-os neutralizációs titert (VNT50) a fluoreszcens virális gócok számának 50%-os csökkenését eredményező hígítás értékének reciprokából becsültük.
VSV-SARS-CoV-2 S-variáns pszeudovírus-neutralizációs eljárás.
A vezikuláris sztomatitisz vírus (VSV)-SARS-CoV-2-S-pszeudorészecskék létrehozása és vizsgálata a neutralizációs eljárással a korábbiakban leírt módon történt24. Röviden, a humán kodonhasználatra optimalizált SARS-CoV-2 S-fehérjét (GenBank azonosító: MN908947.3) szintetizáltuk (Genescript) és egy expressziós plazmidba klónoztuk. A SARS-CoV-2 teljes genomszekvenciáját a GISAID nukleotid-adatbázisból (https://www.gisaid.org) töltöttük le. A szekvenciákat ellenőriztük, majd a jó minőségű genomok segítségével nyert S-gén diverzitását egy saját módszerrel mértük fel. Az S-fehérjét kifejező plazmidon célzott mutagenezis segítségével hoztunk létre aminosavcseréket. A HEK293T-sejteket (ATCC CRL-3216) szélesztettük (sejtkultúra médium: magas glükóztartalmú DMEM [Life Technologies] 10%-os hőinaktivált FBS-sel (Life Technologies) és penicillinnel/sztreptomicinnel/L-glutaminnal [Life Technologies] kiegészítve), majd a következő napon transzfektáltuk az S-fehérjét kifejező plazmiddal Lipofectamine LTX (Life Technologies) segítségével a gyártó utasításainak megfelelően. 24 órával a transzfekciót követően a 37°C-os hőmérsékleten tartott sejteket megfertőztük az Opti-MEM-ben (Life Technologies) felvett egyes multiplicitásnak megfelelő mennyiségű VSVΔG:mNeon/VSV-G-vel. A sejteket 1 órán keresztül 37°C-on inkubáltuk, majd mostuk a feleslegben maradt vírusokat. Ezt követően a fertőzést elősegítő tápoldatottal fedtük (magas glükóztartalmú DMEM 0,7%-os, alacsony IgG-tartalmú marha szérumalbuminnal [BSA, Sigma], nátrium-piruváttal [Life Technologies] és 0,5%-os gentamicinnel [Life Technologies] kiegészítve). 24 órás 37°C-os inkubációt követően a VSV-SARS-CoV-2-S-pszeudorészecskéket tartalmazó tápoldatot összegyűjtöttük, a feltisztulás érdekében 3000 g-n centrifugáltuk 5 percig, majd -80°C-on tároltuk a további felhasználásig.
A pszeudovírus neutralizációs eljáráshoz a Vero-sejteket (ATCC CCL-81) 96-lyukú lemezre szélesztettük tápoldatban, majd megvártuk, míg a sejtek elérik a 85%-os konfluenciát (24 óra alatt) a vizsgálat megkezdéséhez. A szérum hígítási sor 1:2-es arányú lépésekben készült a fertőzést elősegítő tápoldatban, 1:300-as kezdeti hígításból kiindulva. A VSV-SARS-CoV-2-S-pszeudorészecskéket 1:1 arányban hígítottuk a fertőzést elősegítő tápoldattal annak érdekében, hogy a fluoreszcensgóc-egységek (ffu) száma a vizsgálat során kb. 1000 legyen. A szérum hígítási sor egyes lépéseit és a pszeudorészecskéket tartalmazó oldatot 1:1 arányban kevertük 30 percig szobahőmérsékleten, mielőtt a Vero-sejtekhez adtuk őket és megkezdtük a 24 órás inkubációt 37°C-on. A felülúszót eltávolítottuk és PBS-re (Gibco) cseréltük, a fluoreszcens gócokat MiniMax képalkotó citométert (Molecular Devices) tartalmazó SpectraMax i3 lemezolvasóval számoltuk. A neutralizációs titereket a 8.4.2-es verziószámú GraphPad Prism szoftverrel számoltuk a szérum egyes koncentrációin mérhető neutralizációs képesség százalékos értékére illesztett négyparaméteres logisztikus (4PL) illesztésű modellekkel. Az 50%-os pszeudovírus-neutralizációs titert (pVNT50) a fluoreszcens virális gócok számának 50%-os csökkenését eredményező hígítás értékének reciprokából becsültük.
IFNγ ELISpot.
Az IFNγ ELISpot elemzést ex vivo végeztük (az osztódást eredményező további in vitro tenyésztés nélkül) CD4+ T-sejtektől mentes és CD8+ T-sejtekben (CD8+ effektor T-sejtekben) gazdag, valamint CD8+ T-sejtektől mentes és CD4+ T-sejtekben gazdag PBMC-ket használva. A vizsgálatokat kétszer duplikálva végeztük, a pozitív kontroll (anti-CD3) monoklonális antitest jelenlétében [1:1000 hígításban, Mabtech]). Az IFN-specifikusantitestekkel (ELISpotPro kit, Mabtech) bevont szűrős lemezeket PBS-sel mostuk és 2%-os humán szérum albumint tartalmazó X-VIVO 15 oldattal (Lonza) blokkoltuk 1–5 órán át. Lyukanként 3,3×105 effektorsejtet stimuláltunk 16–20 órán keresztül a vad típusú SARS-CoV-2 S-szekvenciájának három különböző részét reprezentáló peptidkészlettel (N-terminális 1-es S-pool [aa 1–643], RBD [aa 1–16 és 327–528 fúziója], valamint C-terminális 2-es S-pool [aa 633–1275]). A megkötött IFN-okat alkalikus foszfatázzal konjugált másodlagos antitestekkel tettük láthatóvá, melyeket 5-bromo-4-kloro-3’-indolil-foszfát (BCIP) vagy nitrokék-tetrazolium (NBT) szubsztráttal inkubáltunk (ELISpotPro kit, Mabtech). A lemezeket AID Classic Robot ELISPOT Readerrel olvastuk le és AID ELISPOT 7.0 szoftverrel (AID Autoimmun Diagnostika) elemeztük. A kapott pöttyök számértékét a duplikált mérések átlagaként ábrázoltuk. A peptidek által stimulált T-sejt-válaszok vizsgálatának negatív kontrolljai olyan effektorok voltak, melyekhez csak tápoldatot adtunk. Az összehasonlítást egy belső fejlesztésű ELISpot adatelemző eszközzel (EDA) végeztük, amelynek alapja a korábban Moodie és munkatársai40,41 által leírt két statisztikai eljárás volt (eloszlásfüggetlen újramintavételezés) annak érdekében, hogy megfelelő érzékenységet érjünk el az álpozitívok számának alacsonyan tartása mellett.
Azért, hogy a különböző alanyoktól származó pöttyszámokat és a reakciók erősségét közvetlenül összehasonlíthassuk, egy normalizációs eljárást alkalmaztunk, amely figyelembe veszi a minták eltérő minőségét, amely az anti-CD3 antitest stimulációra adott válaszként megjelenő pöttyök számában mutatkozik meg. Ezt az összefüggést egy zajkomponenst is tartalmazó loglineáris bayes-i modell segítségével írtuk le (nem publikált). A robosztus normalizáció érdekében minden normalizáció során 10 000-szer mintavételeztünk a modellből és ezek mediánját vettük a pöttyértéknek. A modell valószínűsége: log λE = α log λP + log βj + σε, ahol λE a minta normalizált pöttyértéke, α: egy, az összes pozitív kontroll esetében azonos stabil állandó (amely normál eloszlású), λP és βj a j-edik mintára specifikus komponensek (normál eloszlásúak) és σε a zajkomponens, amelyből az σ Cauchy-eloszlást, az ε pedig Student-féle t-eloszlást mutat. βj biztosítja, hogy minden mintát különböző csoportként kezeljünk.
Áramlási citometria.
A citokintermelő T-sejteket intracelluláris citokinfestéssel azonosítottuk. A PMBC-ket kiolvasztottuk és 4 órán keresztül pihenni hagytuk 2 µg/ml DNáz I-gyel (DNase I, Roche) kiegészített OpTmizer tápoldatban. Ezt követően az ELISpot részben leírt összetételű (2 µg/ml/peptid; JPT Peptide Technologies), az VSV-SARS-CoV-2 S vad típusú peptidszekvencia-készletet különböző mértékben tartalmazó eleggyel újra stimuláltuk GolgiPlug (BD) jelenlétében 18 órán keresztül, 37 °C-on. A kontrollokat DMSO-t tartalmazó tápoldattal kezeltük. A sejteket 20 percig 4°C-on festettük az életképesség és a felszíni markerek jelenlétének vizsgálata céljából (CD3 BV421, 1:250; CD4 BV480, 1:50; CD8 BB515, 1:100; az összes anyag a BD Biosciencestől) az áramlási citométer pufferének jelenlétében (DPBS [Gibco] 2% FBS-sel és [Biochrom], 2 mM etiléndiamin-tetraacetáttal [EDTA; Sigma-Aldrich] kiegészítve). Ezt követően a mintákat fixáltuk és permeabilizáltuk a Cytofix/Cytoperm kit (BD Biosciences) segítségével a gyártó utasításainak megfelelően. Az intracelluláris festést 30 percig végeztük 4°C-on Perm/Wash pufferrel (CD3 BV421, 1:250; CD4 BV480, 1:50; CD8 BB515, 1:100; IFNγ PECy7, 1:50 [HCShez]; IFNγ BB700, 1:250 [a részvevők mintái esetében]; IL-2 PE, 1:10; IL-4 APC, 1:500; az összes anyag a BD Biosciencestől származott). A mintákat fluoreszcenciaaktivált sejtválogatóval (FACS) nyertük ki a VERSE instrument készüléket használva (BD Biosciences), és a 10.6.2-es verziószámú FlowJo (FlowJo LLC, BD Biosciences) szoftverrel elemeztük. Az S- és RBD-specifikus citokintermelést a háttérre korrigáltuk azáltal, hogy a dimetil-szulfoxid tartalmú közegen mért értékeket kivontuk belőlük. A negatív értékeket nullára állítottuk. A 4.b ábrán látható citokintermelést úgy számítottuk, hogy összeadtuk azoknak a CD4+ T-sejteknek a számát, amelyek IFNγ-, IL-2- vagy IL-4-termelést mutattak, ez jelentette a 100%-ot. Az egyes citokineket termelő sejtek részarányát ezen sejtek és az összes sejt számának hányadosa jelenti. A színezett grafikonok tengelyei 10-es alapú logaritmikus beosztásúak.
A peptidek és MHC-multimerek festése.
A multimeranalízishez az MHC-I-epitópokat tömegspektrometria alapú kötődési- és bemutatásiképesség-predikciós módszer42,43 segítségével választottuk ki, úgy, hogy a SARS-CoV-2 tüske-glikoprotein 8–12 aminosav hosszúságú részleteit elemeztük, amelyhez a szekvenciát a GeneBank adatbázisból töltöttük le, (azonosító: NC_045512.2, https://www.ncbi.nlm.nih.gov/nuccore/NC_045512), majd ezeket az európai populációban legalább 5%-os gyakorisággal előforduló 18 MHC-I alléllel állítottuk párba. A predikciók alapján a legjobban kötődő (legfelső 1%) és a legjobban prezentálódó (predikált érték ≥10-2,2) epitópokat azonosítottuk. A legyártott peptidek legalább 90%-os tisztaságúak voltak. A pMHC komplexeket újra foldoltuk az easYmer technológia (easYmer® kit, ImmuneAware Aps) segítségével és a komplexképződést gyöngyalapú áramlási citometriával ellenőriztük a gyártó utasításainak megfelelően44,45. Kombinatorikus jelölést alkalmaztunk a T-sejtek antigén-specificitásának elkülönítéséhez, amely során a sejteket öt különböző fluoreszcens festék kettős kombinációival jelöltünk, lehetővé téve akár 10 különböző T-sejt-populáció azonosítását46. A tetramerizáció érdekében sztreptavidin(SA)-fluorokróm konjugátumokat használtunk: SA BV421, SA BV711, SA PE, SA PE-Cy7, SA APC (az összes anyag a BD Biosciencestől származott). A három BNT162b2-vel oltott résztvevő esetében az egyedi pMHC multimer festődési keveréke tíz különböző pMHC-komplexet tartalmazott, amelyek mindegyike egy egyedi kétszínű jelölést kapott. A PBMC-ket (2×106) 20 percig festettük szobahőmérsékleten ex vivo körülmények között, mindegyik pMHC multimerkeverék végkoncentrációja 4 nM volt Brilliant Staining Buffer Plus pufferben (BSB Plus [BD Horizon™]). A felszíni paramétereket és életképességet kimutató festéseket az áramlási citométer pufferében végeztük (DPBS [Gibco] 2%-os FBS-sel [Biochrom], 2 mM EDTA jelenlétében [Sigma-Aldrich]) BSB Plusszal kiegészítve 30 percig 4°C-on (CD3 BUV395, 1:50; CD45RA BUV563, 1:200; CD27 BUV737, 1:200; CD8 BV480, 1:200; CD279 BV650, 1:20; CD197 BV786, 1:15; CD4 BB515, 1:50; CD28 BB700, 1:100; CD38 PE-CF594, 1:600; HLADR APC-R700, 1:150; az összes anyag a BD Biosciencestől származott; DUMP csatorna: CD14 APC-eFluor780, 1:100; CD16 APC-eFluor780, 1:100; CD19 APC-eFluor780, 1:100; fixálható, életképességet jelző festék eFluor780, 1:1,667; az összes anyag a ThermoFisher Scientific-től származott). A sejteket 15 percig 4°C-on fixáltuk 1-szeres Stabilization Fixative (BD) oldatban, majd FACSymphony™ A3 áramlási citométerrel (BD Biosciences) gyűjtöttük és a 10.6.2-es verziószámú FlowJo szoftverrel (FlowJo LLC, BD Biosciences) elemeztük. A CD8+ T-sejtek reaktivitását akkor tekintettük pozitívnak, ha egy klaszterbe tömörült populáció volt megfigyelhető, amely csak két pMHC színnel volt jelölve.
Statisztikai elemzés.
A vizsgálatban közölt mintaelemszámot nem statisztikai hipotézisvizsgálattal határoztuk meg. Minden résztvevőt bevontunk a biztonságossági- és immunogenitási elemzésekbe, akinek rendelkezésre álltak a megfelelő adatai. Az antitest-koncentrációk és titerek számolása során az értékeket a geometriai átlag és a hozzá tartozó 95%-os konfidenciaintervallum segítségével aggregáltuk. A geometriai átlag használata lehetséges az antitest-koncentrációk és -titerek több nagyságrendet lefedő, nem normál eloszlása esetén is. A nem normál eloszlású adatsorok közti monoton összefüggések leírására Spearman-korrelációt használtunk.
Az összes statisztikai elemzést a 8.4.2-es verziószámú GraphPad Prism programmal végeztük.
Az adatok hozzáférhetősége.
A vizsgálat eredményeit alátámasztó adatokat a levelező szerző bocsájtja rendelkezésre észszerű kérések esetén. Ennek a klinikai vizsgálatnak a lezárulásával az eredmények összefoglalóját nyilvánosságra hozzuk az adatközlés irányelveivel összhangban.
Kibővített adatábrák és -táblázatok
1. kibővített adatábra | Az oltás és az értékelés ütemezése
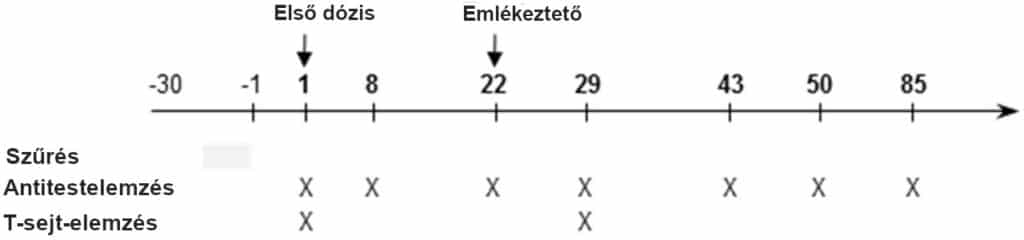
(emlékeztető előtt), a 29±3., a 43±4., az 50±4. és a 85±7. (emlékeztető után) napon nyertük. PBMC-ket az 1. napon (a kezelés előtt) és a 29±3. napon (az emlékeztető után) vizsgáltuk.
2. kibővített adatábra | Vizsgálat keretén belül jelentett nemkívánatos események
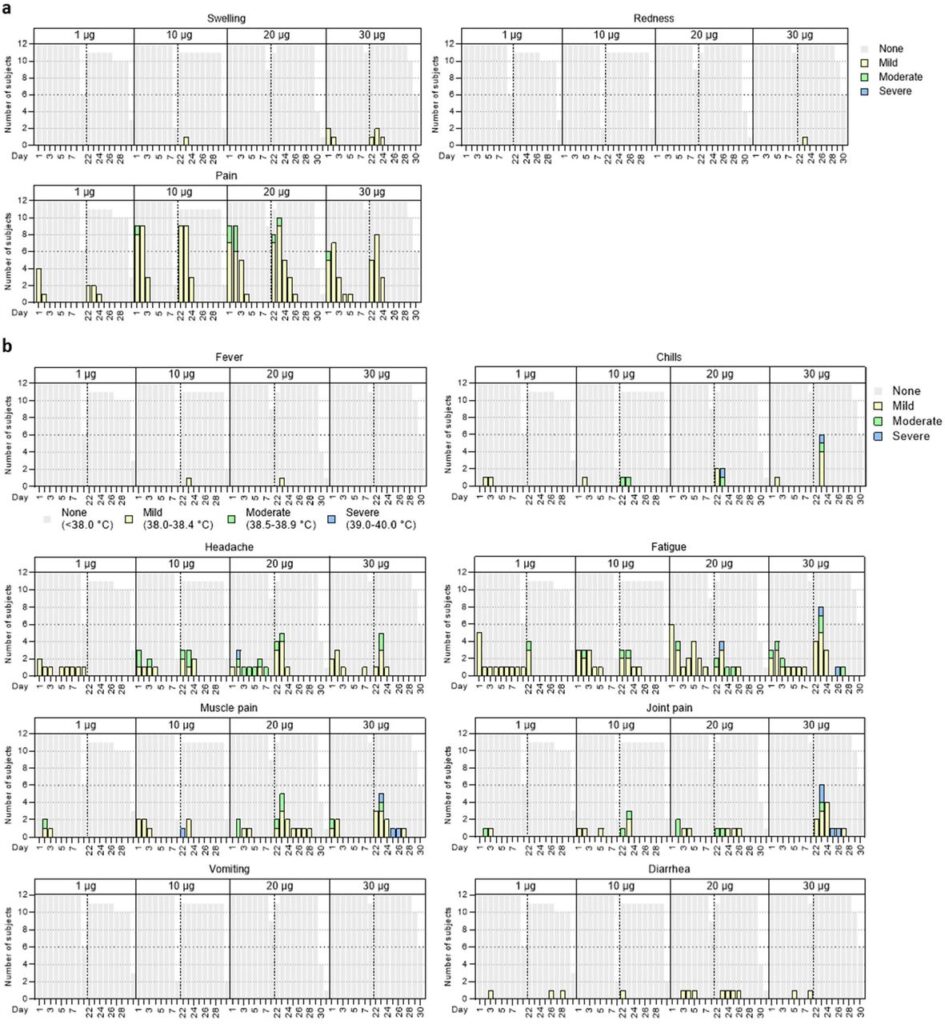
A vizsgálat keretén belül jelentett helyi (a) vagy szisztémás (b) nemkívánatos események (AE) a résztvevők száma szerint. A résztvevőket BNT162b2-vel immunizáltuk az 1. és 22. napon (első oltás n=12 dózis kohorszonként, 1 és 10 µg-os emlékeztető oltás esetén n=11; a résztvevők kizárása nem az oltással összefüggésben lévő okok miatt történt). A szürke árnyékolás a résztvevők számát jelöli az egyes időpontokban. A protokollnak megfelelően az AE-értékeket minden immunizációt követő 7. napig jegyeztük (1-7. és 22-28. napok) a reaktogenitás meghatározása érdekében; bizonyos résztvevők esetében további 1–3 napig tartó utánkövetést végeztünk. A mellékhatások osztályozását az Egyesült Államok Élelmiszer- és Gyógyszerügyi Hatósága (FDA) ajánlásaival összhangban végeztük.
3 kibővített adatábra | Farmakodinamikai markerek
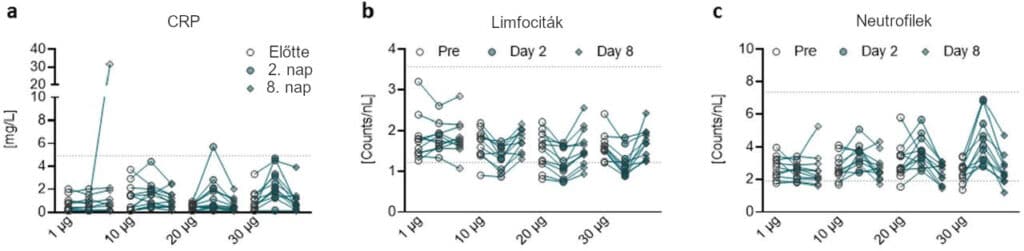
A résztvevőket az 1. és a 22. napon immunizáltuk BNT162b2-vel (n=12 dózis kohorszonként). Egy részvevő az 1 µg-os dózis kohorszban (kiugró érték a 8. napon [a] és a legmagasabb érték a [b] adatsorban) a kezeléssel nem összefüggésben lévő gasztroenteritiszben szenvedett a 6-tól a 8. napig. a, A C-reaktív protein (CRP) szintjének kinetikája. b, A limfocitaszámok kinetikája. c, A neutrofilszámok kinetikája. A pontozott vonalak a referenciatartomány alsó és felső határát jelölik. A beválogatási küszöbérték (LLOQ = 0,3) alá eső értékek esetén az LLOQ/2 értékeket ábrázoltuk (a).
4. kibővített adatábra | A BNT162b2 kiváltotta RBD-specifikus IgG-koncentrációk

5. kibővített adatábra | BNT162b2 indukálta S-specifikus CD8+ és CD4+ T-sejtek
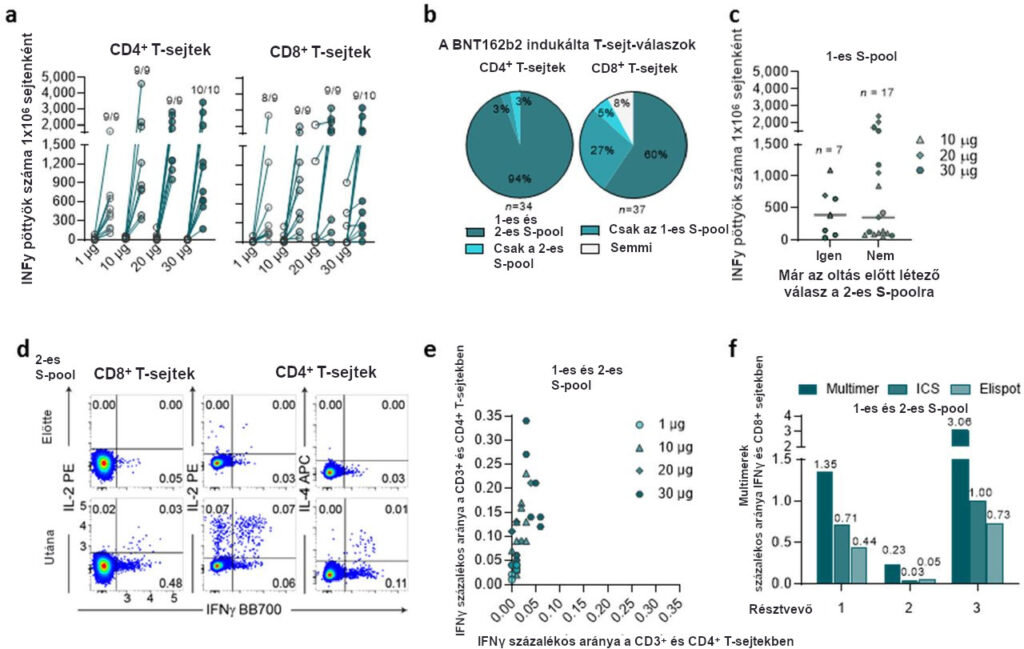
Az 1. napon (az első oltás előtt) és a 29. napon (7 nappal az emlékeztető után) nyert PBMC-ket (1, 10, és 20 µg dózis kohorsz esetén n=9; 30 µg-os dózis kohorsz esetén, n=10) CD4+ vagy CD8+ effektor T-sejtekkel dúsítottuk, és egész éjszakán át külön-külön stimuláltuk három, egymást átfedő peptidkészlettel, amelyek a SARS-CoV-2 S vad típusú szekvenciájának különböző részeit reprezentálták (N-terminális 1-es S-pool és RBD, valamint a C-terminális 2-es S-pool), közvetlenül ex vivo IFNγ ELISpot-tal történő értékelés céljából (a-c). Minden pont a két mérésből származó pontértékek normalizált átlagát jelenti, miután kivontuk belőlük a csak médiumot tartalmazó kontroll értékét. Az 1-es és 2-es S-poollal szembeni T-sejt-válaszokat résztvevőnként összevontuk. Két, a 20 µg-os dózis kohorszba tartozó résztvevő pontértékét nem lehetett normalizálni, ezért nem ábrázoltuk őket. A beoltott résztvevőkből származó 29. napi (7 nappal az emlékeztető oltás után) (1 µg-os dózis kohorsz, n=7; 10 és 30 µg, n=10, 20 µg, n=9) PBMC-ket a fent leírtak szerint stimuláltuk, majd áramlási citometriával vizsgáltuk (d, e). a, S-specifikus CD4+ és CD8+ T-sejt-válaszok minden dóziskohorsznál. A 29. napon detektálható T-sejt-válaszokkal rendelkező résztvevők száma és az összes vizsgált résztvevő száma dózis kohorszonként. b, Az értékelhető kiindulási adatokkal rendelkező résztvevők (n=34 CD4+ és n=37 CD8+ T-sejt-válaszok esetén) vakcinaindukált válaszainak részaránya az S-poolok különböző kombinációihoz viszonyítva. A de novo indukált vagy amplifikált válaszokat a BNT162b2-re adott válaszoknak tekintettük; az oltásra adott válasz hiányát vagy már meglévő, de nem erősödő válaszokat a válasz hiányának minősítettük (nincs jelölés). c, Az 1-es S-poolra adott válaszok erőssége a 2-es S-poolra már fennálló válaszok jelenlétének, vagy hiányának függvényében. Az 1 µg-os dózis kohorszból származó adatpontokat kizártuk, mivel a 2-es S-poolra nem álltak rendelkezésre kezdeti válaszértékek ebben a csoportban. A vízszintes sávok az egyes csoportok mediánját jelölik. d, Példák a 30 µg-os dózisú BNT162b2-vel először/emlékeztetőként beoltott csoport résztvevőinek citokintermelő CD4+ és CD8+ T-sejtjeinek színezett áramlási citometriás ábráira. e, A vakcinaindukált S-specifikus IFNγ+ CD4+ T-sejtek és az IL4+ CD4+ T-sejtek gyakoriságának összefüggése. Az ICS-stimuláció az 1-es és 2-es típusú peptidkészletek keverékével történt. Minden adatpont a tanulmány egyetlen résztvevőjét jelképezi (1 µg-os dózis kohorsz, n=8; 20 µg, n=8; 10 és 30 µg, n=10). A 20 µg-os dózis kohorsz egy résztvevőjének erős, az oltás előtt már fennálló CD4+ T-sejt-válasza volt a 2-es típusú S-pool ellen, ezért kizártuk az elemzésből. f, Az antigénspecifikus CD8+ T-sejt-válaszok gyakorisága, amelyet a pMHC I. multimerfestéssel (multimerek %-os aránya a CD8+ sejtek között), ICS-sel és ELISpot vizsgálattal (multimerek %-os aránya a CD8+ sejtek között) határoztunk meg a 4. ábrán bemutatott három résztvevő esetében. A kapott jeleket összevontuk az 1-es és 2-es S-poolok esetében.
6. kibővített adatábra | Az antitestes és T-sejt-válaszok közti korrelációk

A 29. napon mért értékeket az összes első/emlékeztető oltást kapó résztvevő esetén ábrázoltuk (dózis kohorszok 1, 10, 20 és 30 µg). Azoknak a résztvevőknek az adatait, akik nem mutattak mérhető T-sejt-választ (üres körök a b és c ábrákon) kihagytuk a korrelációs elemzésből. S1-specifikus IgG-válaszok hasonlóan az 1.a ábrához; S-specifikus T-sejt-válaszok az 5.a kibővített ábra a panelén láthatóhoz hasonlóan (n=37). Nem parametrikus Spearman-korreláció. a, Korreláció az S1-specifikus IgG-válaszok és az S-specifikus CD4+ T-sejt-válaszok között. b, Korreláció az S-specifikus CD4+ és CD8+ T-sejt-válaszok között. c, Az S1-specifikus IgG-válaszok korrelációja az S-specifikus CD8+ T-sejt-válaszokkal.
1. kibővített adattáblázat | Demográfiai jellemzők
1.-tablazatN, a résztvevők száma a megadott csoportban Ez az érték a nevező a különböző százalékszámításokban. n az adott tulajdonsággal bíró csoport résztvevőinek száma.
2. kibővített adattáblázat | A résztvevők eloszlása és az elemzésekhez felállított csoportok
2.-tablazatDózis kohorszonként tizenkét résztvevő kapott első és emlékeztető oltást, kettő kivételével, akiket az emlékeztető oltást megelőzően kizártak a kutatásból, egyiküket a vizsgálati készítménnyel nem összefüggő okból (1 µg-os dóziskohorsz), a másikukat egy nemkívánatos esemény miatt (10 µg-os dóziskohorsz, felső légúti tünet). Biztonságossági elemzés: Azon résztvevők száma, akiknél mindkét oltást követően hét napig mérhető volt a határértékeket elérő reaktivitás. Antitestelemzés: Azon résztvevők száma, akiknél vírusneutralizációs eljárást, valamint S1- és RBD-kötő IgG-antitest-eljárást elvégeztük. T-sejt-vizsgálat: Azon résztvevők száma, akiknél rendelkezésre állt a határértéket elérő PBMC az IFNγ ELISpot és az áramlási citometriás (zárójelben) vizsgálatokhoz. N/A, nem értékelhető. *8 és **7 a CD4+ T-sejt-válaszokhoz
3.a kibővített adattáblázat | A vizsgálat keretén belül jelentett helyi reakciók összegzése.
3.-tablazat3.b kibővített adattáblázat | A vizsgálat keretén belül jelentett szisztémás reakciók összegzése
4.-tablazatAz egyesített intervallum az „1. dózis a 7. napig az 1. dózis után” és a „2. dózis a 7. napig a 2. dózis után” metszete. N = az elemzési halmaz résztvevőinek száma; n = azon résztvevőknek a száma, akiknél helyi (a) vagy szisztémás (b) reakció lépett fel; nn = azon résztvevőknek a száma, akiknél bármilyen információ rendelkezésre állt helyi (a) vagy szisztémás (b) reakciókra vonatkozóan.
Hivatkozások
- 1.↵Walsh, E. E. et al. Safety and Immunogenicity of Two RNA-Based Covid-19 Vaccine Candidates. N. Engl. J. Med. NEJMoa2027906 (2020). doi:10.1056/NEJMoa2027906 CrossRef Google Scholar
- 2.↵Pardi, N. et al. Nucleoside-modified mRNA vaccines induce potent T follicular helper and germinal center B cell responses. J. Exp. Med. 215, 1571–1588 (2018).Abstract/FREE Full Text Google Scholar
- 3.↵Rauch, S., Jasny, E., Schmidt, K. E. & Petsch, B. New Vaccine Technologies to Combat Outbreak Situations. Front. Immunol. 9, (2018).Google Scholar
- 4.Pardi, N. et al. Expression kinetics of nucleoside-modified mRNA delivered in lipid nanoparticles to mice by various routes. J. Control. Release 217, 345–351 (2015).CrossRef PubMed Google Scholar
- 5.↵Sahin, U., Kariko, K. & Tureci, O. mRNA-based therapeutics – developing a new class of drugs. Nat. Rev. Drug Discov. 13, 759–780 (2014).CrossRef PubMed Google Scholar
- 6.↵Pardi, N. et al. Nucleoside-modified mRNA immunization elicits influenza virus hemagglutinin stalk-specific antibodies. Nat. Commun. 9, 3361 (2018).CrossRef PubMed Google Scholar
- 7.Pardi, N. et al. Zika virus protection by a single low-dose nucleoside-modified mRNA vaccination. Nature 543, 248–251 (2017).CrossRef PubMed Google Scholar
- 8.↵Pardi, N. et al. Characterization of HIV-1 nucleoside-modified mRNA vaccines in rabbits and rhesus macaques. Mol. Ther. – Nucleic Acids 15, 36–47 (2019).Google Scholar
- 9.↵Mulligan, M. J. et al. Phase 1/2 study of COVID-19 RNA vaccine BNT162b1 in adults. Nature (2020). doi:10.1038/s41586-020-2639-4CrossRef PubMed Google Scholar
- 10.↵Sahin, U. et al. COVID-19 vaccine BNT162b1 elicits human antibody and TH1 T-cell responses. Nature (2020). doi:10.1038/s41586-020-2814-7CrossRef PubMed Google Scholar
- 11.↵Holtkamp, S. et al. Modification of antigen-encoding RNA increases stability, translational efficacy, and T-cell stimulatory capacity of dendritic cells. Blood 108, 4009–4017 (2006).Abstract/FREE Full Text Google Scholar
- 12.↵Orlandini von Niessen, A. G. et al. Improving mRNA-Based Therapeutic Gene Delivery by Expression-Augmenting 3′ UTRs Identified by Cellular Library Screening. Mol. Ther. 27, 824–836 (2019).CrossRef Google Scholar
- 13.↵Karikó, K. et al. Incorporation of pseudouridine into mRNA yields superior nonimmunogenic vector with increased translational capacity and biological stability. Mol. Ther. 16, 1833–40 (2008).CrossRef PubMed Web of Science Google Scholar
- 14.↵Wrapp, D. et al. Cryo-EM structure of the 2019-nCoV spike in the prefusion conformation. Science 367, 1260–1263 (2020).Abstract/FREE Full Text Google Scholar
- 15.↵BNT162b vaccines are immunogenic and protect non-human primates against SARS-CoV-2. Nature in revisio, (2020).Google Scholar
- 16.↵Sahin, U. et al. An RNA vaccine drives immunity in checkpoint-inhibitor-treated melanoma. Nature 585, 107–112 (2020).Google Scholar
- 17.↵Kamphuis, E., Junt, T., Waibler, Z., Forster, R. & Kalinke, U. Type I interferons directly regulate lymphocyte recirculation and cause transient blood lymphopenia. Blood 108, 3253–61 (2006).Abstract/FREE Full Text Google Scholar
- 18.↵Tsai, M. Y. et al. Effect of influenza vaccine on markers of inflammation and lipid profile. J. Lab. Clin. Med. 145, 323–7 (2005).CrossRef PubMed Google Scholar
- 19.Taylor, D. N. et al. Development of VAX128, a recombinant hemagglutinin (HA) influenza-flagellin fusion vaccine with improved safety and immune response. Vaccine 30, 5761–9 (2012).CrossRef PubMed Google Scholar
- 20.Doener, F. et al. RNA-based adjuvant CV8102 enhances the immunogenicity of a licensed rabies vaccine in a first-in-human trial. Vaccine 37, 1819–1826 (2019).Google Scholar
- 21.↵Destexhe, E. et al. Evaluation of C-reactive protein as an inflammatory biomarker in rabbits for vaccine nonclinical safety studies. J. Pharmacol. Toxicol. Methods 68, 367–73 (2013).Google Scholar
- 22.↵Kaech, S. M., Wherry, E. J. & Ahmed, R. Effector and memory T-cell differentiation: implications for vaccine development. Nat. Rev. Immunol. 2, 251–62 (2002).CrossRef PubMed Web of Science Google Scholar
- 23.↵Pérez-Mazliah, D., Ndungu, F. M., Aye, R. & Langhorne, J. B-cell memory in malaria: Myths and realities. Immunol. Rev. 293, 57–69 (2020).CrossRef PubMed Google Scholar
- 24.↵Baum, A. et al. Antibody cocktail to SARS-CoV-2 spike protein prevents rapid mutational escape seen with individual antibodies. Science 369, 1014–1018 (2020).Abstract/FREE Full Text Google Scholar
- 25.↵Zhang, L. et al. The D614G mutation in the SARS-CoV-2 spike protein reduces S1 shedding and increases infectivity. bioRxiv Prepr. Serv. Biol. (2020). doi:bioRxiv: 10.1101/2020.06.12.148726Abstract/FREE Full Text Google Scholar
- 26.↵Sette, A. et al. Selective CD4+ T cell help for antibody responses to a large viral pathogen: deterministic linkage of specificities. Immunity 28, 847–58 (2008).CrossRef PubMed Web of Science Google Scholar
- 27.↵Cameron, M. J., Bermejo-Martin, J. F., Danesh, A., Muller, M. P. & Kelvin, D. J. Human immunopathogenesis of severe acute respiratory syndrome (SARS). Virus Res. 133, 13–9 (2008).CrossRef PubMed Google Scholar
- 28.↵Tang, F. et al. Lack of peripheral memory B cell responses in recovered patients with severe acute respiratory syndrome: a six-year follow-up study. J. Immunol. 186, 7264–8 (2011).Abstract/FREE Full Text Google Scholar
- 29.↵Channappanavar, R., Fett, C., Zhao, J., Meyerholz, D. K. & Perlman, S. Virus-specific memory CD8 T cells provide substantial protection from lethal severe acute respiratory syndrome coronavirus infection. J. Virol. 88, 11034–44 (2014).Abstract/FREE Full Text Google Scholar
- 30.↵Ni, L. et al. Detection of SARS-CoV-2-Specific Humoral and Cellular Immunity in COVID-19 Convalescent Individuals. Immunity 52, 971-977.e3 (2020).Google Scholar
- 31.Grifoni, A. et al. Targets of T Cell Responses to SARS-CoV-2 Coronavirus in Humans with COVID-19 Disease and Unexposed Individuals. Cell 181, 1489-1501.e15 (2020).CrossRef PubMed Google Scholar
- 32.↵Giménez, E. et al. SARS-CoV-2-reactive interferon-γ-producing CD8+ T cells in patients hospitalized with coronavirus disease 2019. J. Med. Virol. (2020). doi:10.1002/jmv.26213CrossRef Google Scholar
- 33.↵Braun, J. et al. Presence of SARS-CoV-2 reactive T cells in COVID-19 patients and healthy donors. medRxiv (2020). doi:10.1101/2020.04.17.20061440Abstract/FREE Full Text Google Scholar
- 34.↵Liu, W. J. et al. T-cell immunity of SARS-CoV: Implications for vaccine development against MERS-CoV. Antiviral Res. 137, 82–92 (2017).CrossRef PubMed Google Scholar
- 35.↵Lu, R. et al. Genomic characterisation and epidemiology of 2019 novel coronavirus: implications for virus origins and receptor binding. Lancet (London, England) 395, 565–574 (2020).CrossRef PubMed Google Scholar
- 36.↵Shomuradova, A. S. et al. SARS-CoV-2 epitopes are recognized by a public and diverse repertoire of human T cell receptors. Immunity (2020). doi:10.1016/j.immuni.2020.11.004CrossRef Google Scholar
- 37.↵Peng, Y. et al. Broad and strong memory CD4+ and CD8+ T cells induced by SARS-CoV-2 in UK convalescent individuals following COVID-19. Nat. Immunol. 21, 1336–1345 (2020).Google Scholar
- 38.↵Xie, X. et al. An Infectious cDNA Clone of SARS-CoV-2. Cell Host Microbe 27, 841-848.e3 (2020).Google Scholar
- 39.↵Muruato, A. E. et al. A high-throughput neutralizing antibody assay for COVID-19 diagnosis and vaccine evaluation. bioRxiv Prepr. Serv. Biol. Accepted at Nat Comun. (2020). doi:bioRxiv: 10.1101/2020.05.21.109546Abstract/FREE Full TextGoogle Scholar
- 40.↵Moodie, Z., Huang, Y., Gu, L., Hural, J. & Self, S. G. Statistical positivity criteria for the analysis of ELISpot assay data in HIV-1 vaccine trials. J. Immunol. Methods 315, 121–32 (2006).CrossRef PubMed Web of Science Google Scholar
- 41.↵Moodie, Z. et al. Response definition criteria for ELISPOT assays revisited. Cancer Immunol. Immunother. 59, 1489–501 (2010).CrossRef PubMed Web of Science Google Scholar
- 42.↵Abelin, J. G. et al. Mass Spectrometry Profiling of HLA-Associated Peptidomes in Mono-allelic Cells Enables More Accurate Epitope Prediction. Immunity 46, 315–326 (2017).CrossRef PubMed Google Scholar
- 43.↵Poran, A. et al. Sequence-based prediction of SARS-CoV-2 vaccine targets using a mass spectrometry-based bioinformatics predictor identifies immunogenic T cell epitopes.Genome Med. 12, 70 (2020). Google Scholar
- 44.↵Svitek, N. et al. Use of ‘one-pot, mix-and-read’ peptide-MHC class I tetramers and predictive algorithms to improve detection of cytotoxic T lymphocyte responses in cattle. Vet. Res. 45, 50 (2014). Google Scholar
- 45.↵Leisner, C. et al. One-pot, mix-and-read peptide-MHC tetramers. PLoS One 3, e1678 (2008).CrossRef PubMed Google Scholar
- 46.↵Hadrup, S. R. et al. Parallel detection of antigen-specific T-cell responses by multidimensional encoding of MHC multimers. Nat. Methods 6, 520–6 (2009).CrossRef PubMed Web of Science Google Scholar
- 47.↵U.S. Department of Health and Human Services, Administration, F. and D. & Research,C. for B. E. and. Toxicity grading scale for healthy adult and adolescent volunteers enrolled in preventive vaccine clinical trials. (2007). Available at: https://www.fda.gov/regulatory-information/search-fda-guidance-documents/toxicity-grading-scale-healthy-adult-and-adolescent-volunteers-enrolled-preventive-vaccine-clinical. Google Scholar
